题目内容
在FeCl3溶液与足量的Fe反应中,还原产物与氧化产物的质量之比为( )
| A、1:2 | B、1:3 |
| C、2:1 | D、2:3 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:发生Fe+2FeCl3=3FeCl2,Fe元素的化合价由0升高为+2价,Fe元素的化合价由+3价降低为+2价,以此来解答.
解答:
解:发生Fe+2FeCl3=3FeCl2,Fe元素的化合价由0升高为+2价,失去电子被氧化,对应的FeCl2为氧化产物;
元素的化合价由+3价降低为+2价,得到电子被还原,对应的FeCl2为还原产物,
由电子守恒及原子守恒可知,还原产物与氧化产物的质量之比等于物质的量比,均为2:1,
故选C.
元素的化合价由+3价降低为+2价,得到电子被还原,对应的FeCl2为还原产物,
由电子守恒及原子守恒可知,还原产物与氧化产物的质量之比等于物质的量比,均为2:1,
故选C.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化及基本概念为解答的关键,侧重分析与计算能力的考查,题目难度不大.

练习册系列答案
相关题目
相对分子质量为72的烷烃,其同分异构体有( )种.
| A、3 | B、4 | C、5 | D、6 |
此反应:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,氧化剂和还原剂的物质的量比为( )
| ||
| A、4:1 | B、1:4 |
| C、1:1 | D、1:2 |
下列关于原电池的叙述中,正确的是( )
| A、原电池中,正极就是阳极,负极就是阴极 |
| B、形成原电池时,在负极上发生还原反应 |
| C、原电池工作时,溶液中的阳离子向负极移动 |
| D、电子从负极流向正极 |
如图氧化还原反应中,电子转移的方向和数目均正确的是( )
A、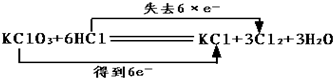 |
B、 |
C、 |
D、 |
实现下列变化,需要加入还原剂的是( )
| A、CO32-→CO2 |
| B、SO2→SO32- |
| C、MnO4-→Mn2+ |
| D、Cl-→Cl2 |
人体正常的血红蛋白中含有Fe2+,若误食亚硝酸盐,则使血红蛋白中Fe2+转化为Fe3+丧失其生理功能,临床证明服用维生素C可以解毒.下列叙述正确的是( )
| A、中毒反应中亚硝酸盐是氧化剂 |
| B、中毒反应中Fe3+是氧化剂 |
| C、维生素C能将亚硝酸盐氧化成硝酸盐,使其解毒 |
| D、维生素C能将Fe3+还原为Fe2+,使其解毒 |
已知14.2gX气体在标准状况下的体积是4.48L,则X气体的摩尔质量是( )
| A、71g |
| B、71 |
| C、71g/mol |
| D、142g/mol |