题目内容
25℃时,下列溶液中有关粒子的物质的量浓度关系正确的是( )
| A、pH=4的HCl溶液与pH=4的醋酸中c(Cl-)>c(CH3COO-) |
| B、20 mL 0.1 mol?L-1氨水与10 mL 0.1 mol?L-1盐酸的混合溶液中c(NH4+)+c(NH3?H2O)=c(Cl-)+c(OH- ) |
| C、pH=8的0.1 mol?L-1的NaHB溶液中c(HB-)>c(H+)>c(B2-)>c (H2B) |
| D、20 mL 0.1 mol?L-1NaHCO3溶液与10 mL 0.1 mol?L-1NaOH溶液混合后c(HCO3-)+3c(H2CO3)-c(CO32-)=2[c(OH-)-c(H+)] |
考点:离子浓度大小的比较
专题:
分析:A、pH=4的HCl溶液与pH=4的醋酸中,c(H+)相等,根据电荷守恒可知c(Cl-)=c(CH3COO-);
B、20 mL 0.1 mol?L-1氨水与10 mL 0.1 mol?L-1盐酸反应生成0.001 mol NH4Cl,同时还余0.001 mol NH3?H2O,故n(NH4+)+n(NH3?H2O)=0.002 mol,一水合氨是弱电解质,且氯化铵对一水合氨的电离起抑制作用,则n(OH- )<0.001 mol,由此得出结论;
C、pH=8的0.1 mol?L-1的NaHB溶液中,HB-的电离程度小于水解程度,所以离子浓度的大小为c(HB-)>c (H2B)>c(H+)>c(B2-);
D、20 mL 0.1 mol?L-1NaHCO3溶液与10 mL 0.1 mol?L-1NaOH溶液发生反应生成0.001 mol Na2CO3,同时还余0.001 mol NaHCO3,电荷守恒式为c(HCO3-)+2c(CO32-)+c(OH-)=c(H+)+c(Na+),物料守恒式为3[c(HCO3-)+c(CO32-)+c(H2CO3)]=2c(Na+),两式消去c(Na+).
B、20 mL 0.1 mol?L-1氨水与10 mL 0.1 mol?L-1盐酸反应生成0.001 mol NH4Cl,同时还余0.001 mol NH3?H2O,故n(NH4+)+n(NH3?H2O)=0.002 mol,一水合氨是弱电解质,且氯化铵对一水合氨的电离起抑制作用,则n(OH- )<0.001 mol,由此得出结论;
C、pH=8的0.1 mol?L-1的NaHB溶液中,HB-的电离程度小于水解程度,所以离子浓度的大小为c(HB-)>c (H2B)>c(H+)>c(B2-);
D、20 mL 0.1 mol?L-1NaHCO3溶液与10 mL 0.1 mol?L-1NaOH溶液发生反应生成0.001 mol Na2CO3,同时还余0.001 mol NaHCO3,电荷守恒式为c(HCO3-)+2c(CO32-)+c(OH-)=c(H+)+c(Na+),物料守恒式为3[c(HCO3-)+c(CO32-)+c(H2CO3)]=2c(Na+),两式消去c(Na+).
解答:
解:A、pH=4的HCl溶液与pH=4的醋酸中,c(H+)相等,根据电荷守恒可知c(Cl-)=c(CH3COO-),故A错误;
B、20 mL 0.1 mol?L-1氨水与10 mL 0.1 mol?L-1盐酸反应生成0.001 mol NH4Cl,同时还余0.001 mol NH3?H2O,故n(NH4+)+n(NH3?H2O)=0.002 mol,一水合氨是弱电解质,且氯化铵对一水合氨的电离起抑制作用,则n(OH- )<0.001 mol,故n(Cl-)+n(OH- )<0.002 mol,故B错误;
C、pH=8的0.1 mol?L-1的NaHB溶液中,HB-的电离程度小于水解程度,所以离子浓度的大小为c(HB-)>c (H2B)>c(H+)>c(B2-),故C错误;
D、20 mL 0.1 mol?L-1NaHCO3溶液与10 mL 0.1 mol?L-1NaOH溶液发生反应生成0.001 mol Na2CO3,同时还余0.001 mol NaHCO3,电荷守恒式为c(HCO3-)+2c(CO32-)+c(OH-)=c(H+)+c(Na+),物料守恒式为3[c(HCO3-)+c(CO32-)+c(H2CO3)]=2c(Na+),两式消去c(Na+),得c(HCO3-)+3c(H2CO3)-c(CO32-)=2[c(OH-)-c(H+)],故D正确;
故选D.
B、20 mL 0.1 mol?L-1氨水与10 mL 0.1 mol?L-1盐酸反应生成0.001 mol NH4Cl,同时还余0.001 mol NH3?H2O,故n(NH4+)+n(NH3?H2O)=0.002 mol,一水合氨是弱电解质,且氯化铵对一水合氨的电离起抑制作用,则n(OH- )<0.001 mol,故n(Cl-)+n(OH- )<0.002 mol,故B错误;
C、pH=8的0.1 mol?L-1的NaHB溶液中,HB-的电离程度小于水解程度,所以离子浓度的大小为c(HB-)>c (H2B)>c(H+)>c(B2-),故C错误;
D、20 mL 0.1 mol?L-1NaHCO3溶液与10 mL 0.1 mol?L-1NaOH溶液发生反应生成0.001 mol Na2CO3,同时还余0.001 mol NaHCO3,电荷守恒式为c(HCO3-)+2c(CO32-)+c(OH-)=c(H+)+c(Na+),物料守恒式为3[c(HCO3-)+c(CO32-)+c(H2CO3)]=2c(Na+),两式消去c(Na+),得c(HCO3-)+3c(H2CO3)-c(CO32-)=2[c(OH-)-c(H+)],故D正确;
故选D.
点评:本题考查溶液中离子的浓度的关系,明确电离、水解及溶液中的电荷守恒、物料守恒是解答本题的关键,本题中的B是易错点,两种守恒的混合应用.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
烯烃复分解反应是指在金属钨或钼等催化剂的作用下,碳碳双键断裂并重新组合的过程.例如:

则对于有机物CH2=CHCH2CH=CH2发生烯烃复分解反应时可能生成产物的判断中正确的是( )
①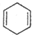 ②CH2=CH2③
②CH2=CH2③ ④CH2=C=CH2.
④CH2=C=CH2.

则对于有机物CH2=CHCH2CH=CH2发生烯烃复分解反应时可能生成产物的判断中正确的是( )
①
 ②CH2=CH2③
②CH2=CH2③ ④CH2=C=CH2.
④CH2=C=CH2.| A、只有③ | B、只有②③ |
| C、只有①②③ | D、有①②③④ |
下列实验能证明一定有二氧化硫存在的是( )
①能使澄清石灰水变浑浊
②能使品红溶液褪色
③能使湿润的蓝色石蕊试纸变红
④通入足量的NaOH溶液,再加入BaCl2溶液有白色沉淀产生,该沉淀溶于盐酸
⑤通入溴水能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀产生.
①能使澄清石灰水变浑浊
②能使品红溶液褪色
③能使湿润的蓝色石蕊试纸变红
④通入足量的NaOH溶液,再加入BaCl2溶液有白色沉淀产生,该沉淀溶于盐酸
⑤通入溴水能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀产生.
| A、都不能 | B、都能 |
| C、②④⑤ | D、只有⑤ |
常温下,柠檬酸水溶液的pH是3,食用醋的pH是2,可乐的pH是6,三种物质的溶液中c(OH-)分别是( )
| A、1×10-11 mol?L-1,1×10-12 mol?L-1,1×10-8 mol?L-1 |
| B、1×10-11 mol?L-1,1×10-8 mol?L-1,1×10-12 mol?L-1 |
| C、2×10-11 mol?L-1,1×10-10 mol?L-1,1×10-8 mol?L-1 |
| D、1×10-8 mol?L-1,1×10-11 mol?L-1,1×10-12 mol?L-1 |
若某池(电解池或原电池)的总反应离子方程式是Cu+2H+═Cu2++H2↑,关于此池的有关说法正确的是( )
| A、该池只能是电解池,且金属铜为该电解池的阳极 |
| B、该池只能是原电池,且电解质溶液为硝酸 |
| C、该池可能是原电池,也可能是电解池 |
| D、该池只能是电解池,电解质溶液可以是硫酸铜 |
下列反应不属于氧化还原反应的是( )
| A、Fe+CuSO4=Cu+FeSO4 | ||||
| B、AgNO3+NaCl=AgCl↓+NaNO3 | ||||
C、3CO+Fe2O3
| ||||
D、MgCl2(熔融)
|
下列物质的水溶液能导电,但属于非电解质的是( )
| A、SO2 |
| B、Cl2 |
| C、NH4HCO3 |
| D、HNO3 |