题目内容
6.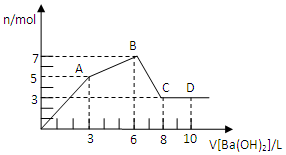 向Al2(SO4)3和AlCl3的混合溶液中逐滴加入1mol/L Ba(OH)2溶液至过量,加入Ba(OH)2溶液的体积和所得沉淀的量的关系如图,下列说法不正确的是( )
向Al2(SO4)3和AlCl3的混合溶液中逐滴加入1mol/L Ba(OH)2溶液至过量,加入Ba(OH)2溶液的体积和所得沉淀的量的关系如图,下列说法不正确的是( )| A. | 图中C点铝元素存在的形式是[Al(OH)4]- | |
| B. | 向D点溶液中通入过量CO2气体,立即产生白色沉淀 | |
| C. | 原混合溶液中c[Al2(SO4)3]:c(AlCl3)=1:2 | |
| D. | OA段反应的离子方程式为:2Al3++3SO42-+3Ba2++8OH-═2Al(OH)4-+3BaSO4↓ |
分析 向含Al2(SO4)3 和 AlCl3的混合溶液与Ba(OH)2溶液反应的实质是Al3+与OH-、Ba2+与SO42-之间的离子反应,如下:
Ba2++SO42-═BaSO4↓,Al3++3OH-═Al(OH)3↓,Al(OH)3+OH-═AlO2-+2H2O,
假设1molAl2(SO4)3中SO42-完全被沉淀所需Ba(OH)2量为3mol,提供6molOH-,1molAl2(SO4)3中含有2molAl3+,由反应Al3++3OH-═Al(OH)3↓可知,2molAl3+完全沉淀,需要6molOH-,故:
从起点到A点,可以认为是硫酸铝与氢氧化钡恰好发生反应生成硫酸钡、氢氧化铝沉淀,A点时SO42-完全沉淀,
A-B为氯化铝与氢氧化钡的反应,B点时溶液中Al3+完全沉淀,产生沉淀达最大值,溶液中溶质为BaCl2,
B-C为氢氧化铝与氢氧化钡反应,C点时氢氧化铝完全溶解,
A、C点时氢氧化铝完全溶解;
B、D点的溶液中含有Ba2+、AlO2-;
C、前3LBa(OH)2溶液与溶液中Al2(SO4)3反应,从3L-6L为Ba(OH)2溶液与溶液中AlCl3反应,据此计算;
D、OA段实质为Ba(OH)2溶液与溶液中Al2(SO4)3反应.
解答 解:向含Al2(SO4)3 和 AlCl3的混合溶液与Ba(OH)2溶液反应的实质是Al3+与OH-、Ba2+与SO42-之间的离子反应,如下:Ba2++SO42-═BaSO4↓,Al3++3OH-═Al(OH)3↓,Al(OH)3+OH-═AlO2-+2H2O,
假设1molAl2(SO4)3中SO42-完全被沉淀所需Ba(OH)2量为3mol,提供6molOH-,1molAl2(SO4)3中含有2molAl3+,由反应Al3++3OH-═Al(OH)3↓可知,2molAl3+完全沉淀,需要6molOH-,故:
从起点到A点,可以认为是硫酸铝与氢氧化钡恰好发生反应生成硫酸钡、氢氧化铝沉淀,A点时SO42-完全沉淀,
A-B为氯化铝与氢氧化钡的反应,B点时溶液中Al3+完全沉淀,产生沉淀达最大值,溶液中溶质为BaCl2,
B-C为氢氧化铝与氢氧化钡反应,C点时氢氧化铝完全溶解,
A、C点时氢氧化铝完全溶解,转化为偏铝酸盐,故C点铝元素存在形式是AlO2-,故A正确;
B、D点的溶液中含有Ba2+、AlO2-,通入二氧化碳立即产生碳酸钡、氢氧化铝沉淀,故B正确;
C、前3LBa(OH)2溶液与溶液中Al2(SO4)3反应,从3L-6L为Ba(OH)2溶液与溶液中AlCl3反应,二者消耗的氢氧化钡的物质的量相等为3L×1mol/L=3mol,由生成硫酸钡可知3n[Al2(SO4)3]=n[Ba(OH)2],故n[Al2(SO4)3]=1mol,由氯化铝与氢氧化钡生成氢氧化铝可知3n(AlCl3)=2[Ba(OH)2]=6mol,故n(AlCl3)=2mol,故原溶液中原混合液中c[Al2(SO4)3]:c(AlCl3)=1:2,故C正确;
D、OA段实质为硫酸铝与氢氧化钡恰好发生反应生成硫酸钡、氢氧化铝沉淀,反应离子方程式为:
3Ba2++2Al3++6OH-+3SO42-=3BaSO4↓+2Al(OH)3↓,故D错误;
故选D.
点评 本题考查化学反应的有关图象问题、铝化合物性质、混合物的有关计算等,难度较大,关键是清楚各阶段发生的反应,注意从开始到A点相当于是硫酸铝与氢氧化钡的反应生成硫酸钡、氢氧化铝沉淀.

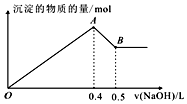 现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )| A. | 1:3 | B. | 3:1 | C. | 2:3 | D. | 6:1 |
 短周期元素A、B、C的位置如图所示,已知B、C两元素所在族序数之和是A元素所在族序数的二倍,B、C两元素的原子序数之和是A元素的4倍,则A、B、C依次是( )
短周期元素A、B、C的位置如图所示,已知B、C两元素所在族序数之和是A元素所在族序数的二倍,B、C两元素的原子序数之和是A元素的4倍,则A、B、C依次是( )| A. | Be、Na、Al | B. | C、Al、P | C. | O、P、Cl | D. | B、Mg、S |
| A. | Al+HCl | B. | Al+H2SO4 | C. | Al+Mg | D. | Al+WO3 |
| A. | SiO2是酸性氧化物不跟任何酸反应 | |
| B. | 水玻璃敞口存放,能有白色胶状沉淀析出 | |
| C. | 高温时SiO2能跟Na2CO3反应放出CO2,所以硅酸的酸性比碳酸强 | |
| D. | SiO2和CO2化学性质虽然相似,且两者的结构完全相同 |
 当前情况下散烧煤和没有清洁的煤是造成中国城市雾霾或者东部雾霾的主要原因,煤的气化是解决雾霾,清洁地利用煤炭的重要途径之一.
当前情况下散烧煤和没有清洁的煤是造成中国城市雾霾或者东部雾霾的主要原因,煤的气化是解决雾霾,清洁地利用煤炭的重要途径之一.(1)已知:H2O(g)=H2O(l)△H=44KJ/mol
| 物质 | H2(g) | C(s) | CO(g) |
| 燃烧热KJ/mol | 285.8 | 393.5 | 283.0 |
②在恒温、恒容的反应器中,能表明上述反应达到平衡状态的是abef.
a.混合气体平均相对分子质量不再改变 b.气体压强不再改变
c.各气体浓度相等 d.反应体系中温度保持不变
e.断裂氢氧键速率是断裂氢氢键速率的2倍 f.混合提前密度不变
g.单位时间内,消耗水的质量与生成氢气的质量比为9:1
(2)甲醇是重要的化工原料,又可作为燃料,工业上利用合成气(主要成分为CO、CO2、H2)在催化剂的作用下合成甲醇,其中部分主要反应如下:
CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H=-58kJ/mol
①请推断该反应自发进行的条件为由于该反应△S<0,△H<0,故根据△G=△H-T△S<0,反应自发,可判断该反应在低温下能自发进行.
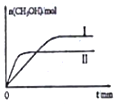
②若将1 mol CO2和2 mol H2充入容积为2L的恒容密闭容器中,在两种不同温度下发生反应,测得CH3OH的物质的量随时间的变化如图所示.曲线Ⅰ、Ⅱ对应的平成常数大小关系为KⅠ>KⅡ(填“>”或“=”或“<”);若5 min后反应达到平衡状态,H2的转化率为90%,则用CO2表示的平均反应速率为0.06mol/(L.min),该温度下的平衡常数为450;若容器容积不变,下列措施可增加甲醇产率的是d.
a.升高温度 b.使用合适的催化剂 c.充入He d.按原比例再充入CO2和H2
③CH4燃料电池利用率很高,装置中添加1L 2mol/L的KOH溶液为电解质,持续缓慢通入标准状况下甲烷2.24L时负极电极反应为CH4-8e-+10OH-=CO32-+7H2O.
| A. | 烧杯 | B. | 铁架台(带铁圈) | C. | 漏斗 | D. | 药匙 |
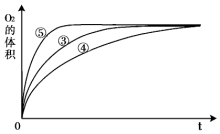 某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如表方案完成实验.
某实验小组以H2O2分解为例,研究浓度、催化剂、溶液酸碱性对反应速率的影响.在常温下按照如表方案完成实验.| 实验编号 | 反应物 | 催化剂 |
| ① | 10mL2% H2O2溶液 | 无 |
| ② | 10mL5% H2O2溶液 | 无 |
| ③ | 10mL5% H2O2溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ④ | 10mL5% H2O2溶液+少量HCl溶液 | 1mL0.1mol•L-1FeCl3溶液 |
| ⑤ | 10mL5% H2O2溶液+少量NaOH溶液 | 1mL0.1mol•L-1FeCl3溶液 |
(2)写出实验③的化学反应方程式2H2O2$\frac{\underline{\;FeCl_{3}\;}}{\;}$O2↑+2H2O.
(3)实验③、④、⑤中,测得生成氧气的体积随时间变化的关系如图.分析上图能够得出的实验结论是碱性环境能增大H2O2分解的速率,酸性环境能减小H2O2分解的速率.