题目内容
17.在6KOH+3Cl2═KClO3+5KCl+3H2O的反应中,下列说法中正确的是( )| A. | Cl2是氧化剂,KOH是还原剂 | |
| B. | KOH是氧化剂,Cl2是还原剂 | |
| C. | KCl是还原产物,KClO3是氧化产物 | |
| D. | 被氧化的氯原子与被还原的氯原子数之比为5:1 |
分析 A、化合价升高元素所处的反应物为还原剂,化合价降低元素所在的反应物为氧化剂;
B、氢氧化钠中各元素的化合价不变,氯气中的氯元素的化合价既升高又降低;
C、化合价升高元素所处的生成物为氧化产物,化合价降低元素所在的生成物为还原产物;
D、根据反应确定氧化剂和还原剂,进而确定它们的量关系.
解答 解:A、化合价变化的元素只有氯元素,氯气既是氧化剂又是还原剂,故A错误;
B、氢氧化钠中各元素的化合价不变,所以氢氧化钠既不是氧化剂也不是还原剂,氯气中的氯元素的化合价既升高又降低,则氯气既是氧化剂又是还原剂,故B错误;
C、KClO3为氧化产物,KCl为还原产物,故C正确;
D、6mol氯原子中,做氧化剂的占5mol,做还原剂的占1mol,所以氧化剂质量是还原剂质量的5倍,被氧化的氯原子与被还原的氯原子数之比为1:5,故D错误.
故选C.
点评 本题考查氧化还原反应的特征和有关的概念内涵,要求学生具有分析和解决问题的能力,注意反应中只有一种元素化合价变化时的情况,难度较大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
17.已知在25℃时,下列反应的平衡常数如下:
①N2(g)+O2(g)??2NO(g) K1=1×10-30
②2H2(g)+O2(g)?2H2O(g) K2=2×1081
③2CO2(g)?2CO(g)+O2(g) K3=4×10-92
下列说法正确的是( )
①N2(g)+O2(g)??2NO(g) K1=1×10-30
②2H2(g)+O2(g)?2H2O(g) K2=2×1081
③2CO2(g)?2CO(g)+O2(g) K3=4×10-92
下列说法正确的是( )
| A. | NO分解反应NO(g)?$\frac{1}{2}$N2(g)+$\frac{1}{2}$O2(g)的平衡常数为1×10-30 | |
| B. | 根据K2的值可以判断常温下H2和O2很容易反应生成H2O | |
| C. | 常温下,NO、H2O、CO2三种物质分解放出O2的倾向顺序为NO>H2O>CO2 | |
| D. | 温度升高,上述三个反应的平衡常数均增大 |
18.有关溶液中所含离子的检验,下列判断正确的是( )
| A. | 加入硝酸酸化,再滴加KSCN溶液后有红色物质生成,则原溶液中一定有Fe3+存在 | |
| B. | 加入盐酸有能使澄清石灰水变浑浊的气体生成,则原溶液中一定有大量的CO32-存在 | |
| C. | 某溶液做焰色反应时火焰为黄色,则该溶液中一定有钠元素 | |
| D. | 分别含有Mg2+、Cu2+、Fe2+和Na+的四种盐溶液,只用NaOH溶液不能一次性鉴别开 |
5.已知苯甲酸微溶于水,易溶于乙醇、乙醚,有弱酸性,酸性比醋酸强.它可用于制备苯甲酸乙酯.
制备苯甲酸乙酯的反应原理
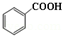 +C2H5OH$\stackrel{H_{2}SO_{4}}{?}$
+C2H5OH$\stackrel{H_{2}SO_{4}}{?}$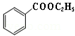 +H2O
+H2O
相关物质的部分物理性质如表格:
实验流程如图1:
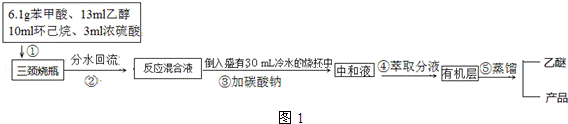
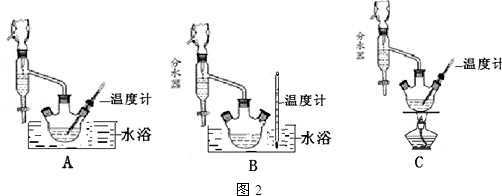
(1)制备苯甲酸乙酯,图2装置最合适的是B,反应液中的环己烷在本实验中的作用带出生成的水,促进酯化反应向正向进行.
(2)步骤②控制温度在65~70℃缓慢加热液体回流,分水器中逐渐出现上、下两层液体,直到反应完成,停止加热.放出分水器中的下层液体后,继续加热,蒸出多余的乙醇和环己烷.
反应完成的标志是分水器中下层(水层)液面不再升高.
(3)步骤③碳酸钠的作用是中和苯甲酸和硫酸,碳酸钠固体需搅拌下分批加入的原因加入过快大量泡沫的产生可使液体溢出.
(4)步骤④将中和后的液体转入分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有机层,用无水MgSO4干燥.乙醚的作用萃取出水层中溶解的苯甲酸乙酯,提高产率.
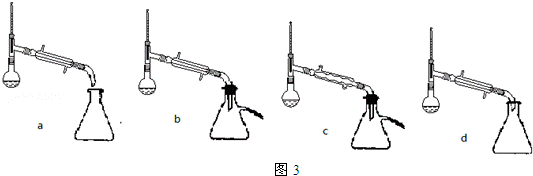
(5)步骤⑤蒸馏操作中,图3装置最好的是b d(填标号),蒸馏时先低温蒸出乙醚,蒸馏乙醚时最好采用水浴加热(水浴加热、直接加热、油浴加热).
(6)最终得到6.75g纯品,则苯甲酸乙酯的产率是90%.
制备苯甲酸乙酯的反应原理
 +C2H5OH$\stackrel{H_{2}SO_{4}}{?}$
+C2H5OH$\stackrel{H_{2}SO_{4}}{?}$ +H2O
+H2O相关物质的部分物理性质如表格:
| 沸点(℃) | 密度(g•cm-3) | |
| 苯甲酸 | 249 | 1.2659 |
| 苯甲酸乙酯 | 212.6 | 1.05 |
| 乙醇 | 78.5 | 0.7893 |
| 环已烷 | 80.8 | 0.7785 |
| 乙醚 | 34.51 | 0.7318 |
| 环已烷、乙醇和水共沸物 | 62.1 |

(1)制备苯甲酸乙酯,图2装置最合适的是B,反应液中的环己烷在本实验中的作用带出生成的水,促进酯化反应向正向进行.

(2)步骤②控制温度在65~70℃缓慢加热液体回流,分水器中逐渐出现上、下两层液体,直到反应完成,停止加热.放出分水器中的下层液体后,继续加热,蒸出多余的乙醇和环己烷.
反应完成的标志是分水器中下层(水层)液面不再升高.
(3)步骤③碳酸钠的作用是中和苯甲酸和硫酸,碳酸钠固体需搅拌下分批加入的原因加入过快大量泡沫的产生可使液体溢出.
(4)步骤④将中和后的液体转入分液漏斗分出有机层,水层用25mL乙醚萃取,然后合并至有机层,用无水MgSO4干燥.乙醚的作用萃取出水层中溶解的苯甲酸乙酯,提高产率.
(5)步骤⑤蒸馏操作中,图3装置最好的是b d(填标号),蒸馏时先低温蒸出乙醚,蒸馏乙醚时最好采用水浴加热(水浴加热、直接加热、油浴加热).

(6)最终得到6.75g纯品,则苯甲酸乙酯的产率是90%.
2.下列离子方程式的书写正确的是( )
| A. | 硫化钠水解:S2-+2H2O?H2S↑+2OH- | |
| B. | 硫氢化钠水解:HS-+H2O?H3O++S2- | |
| C. | 硫化钾水解:S2-+H2O?HS-+OH- | |
| D. | 硫酸铝溶液跟碳酸氢钠溶液反应:Al3++3HCO3-+6H2O?Al(OH)3↓+3CO2↑ |
5.将AgCl 和AgI 的饱和溶液相混合,在其中加入足量AgNO3 固体,将会( )
| A. | 只有AgCl 沉淀 | B. | 只有AgI 沉淀 | ||
| C. | AgCl、AgI 都沉淀,以AgCl 为主 | D. | AgCl、AgI 都沉淀,以AgI 为主 |
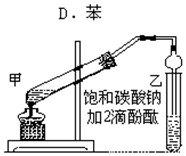 实验室制取乙酸乙酯的主要步骤如下:
实验室制取乙酸乙酯的主要步骤如下: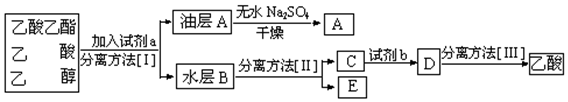
 产物不稳定,受热即脱水而生成不饱和醛.
产物不稳定,受热即脱水而生成不饱和醛.
 ;F
;F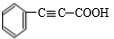 .
. +CH3CHO$\stackrel{△}{→}$
+CH3CHO$\stackrel{△}{→}$ +2NaOH$→_{△}^{乙醇}$
+2NaOH$→_{△}^{乙醇}$