题目内容
2.某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现如图所示的物质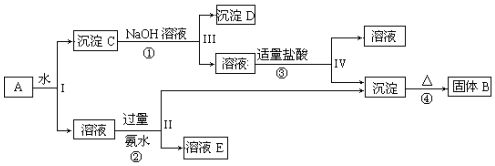
据此回答下列问题:
(1)KAl(SO4)2的电离方程式KAl(SO4)2=K++Al3++2SO42-.
(2)根据上述框图反应关系,写出下列C、E所含物质的化学式沉淀CAl2O3、Fe2O3;溶液EK2SO4、(NH4)2SO4、NH3•H2O.
(3)写出①、②两步的化学反应方程式是
①Al2O3+2NaOH=2NaAlO2+H2O;②2KAl(SO4)2+6NH3•H2O=K2SO4+3(NH4)2SO4+2Al(OH)3↓.
分析 混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,由流程可知,加水溶液、过滤后分离出C含Al2O3和Fe2O3,Al2O3与NaOH反应,则过滤分离出D为Fe2O3,溶液与盐酸发生反应生成沉淀为氢氧化铝,加热生成B为Al2O3,且KAl(SO4)2与氨水反应生成氢氧化铝,加热生成B,溶液E中含硫酸铵、硫酸钾、一水合氨,以此来解答.
解答 解:(1)KAl(SO4)2的电离方程式为KAl(SO4)2=K++Al3++2SO42-,故答案为:KAl(SO4)2=K++Al3++2SO42-;
(2)由上述分析可知,沉淀C含Al2O3、Fe2O3;溶液E含K2SO4、(NH4)2SO4、NH3•H2O,故答案为:Al2O3、Fe2O3;K2SO4、(NH4)2SO4、NH3•H2O;
(3)反应①为Al2O3+2NaOH=2NaAlO2+H2O;反应②为2KAl(SO4)2+6 NH3•H2O=K2SO4+3(NH4)2SO4+2Al(OH)3↓,
故答案为:Al2O3+2NaOH=2NaAlO2+H2O;2KAl(SO4)2+6NH3•H2O=K2SO4+3(NH4)2SO4+2Al(OH)3↓.
点评 本题考查混合物分离提纯的综合应用,为高频考点,把握流程中发生的反应、混合物分离方法为解答的关键,侧重分析与实验能力的考查,注意元素化合物与实验的结合,题目难度不大.

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
5.向烧杯中加入25mL蒸馏水,加热至沸腾,向沸水中逐滴加入6滴FeCl3饱和溶液.继续加热至溶液呈红棕色,停止加热,就制得了Fe(OH)3胶体.下列有关胶体的叙述不正确的是( )
| A. | 胶体是一种分散系,属于混合物 | |
| B. | 胶体的本质特征是能发生丁达尔现象 | |
| C. | 胶体粒子直径介于1nm-100nm | |
| D. | 利用丁达尔现象是区分胶体和溶液的一种常用方法 |
13.用NA表示阿伏伽德罗常数的值,下列叙述正确的是( )
| A. | 100ml0.1mol•L-1Na2SO4溶液中,微粒总数是0.03NA | |
| B. | 标准状况下,分子数为NA的N2、C2H4混合气体的质量无法确定 | |
| C. | 常温常压下,32g O2-中所含电子的数目为17NA | |
| D. | 标准状况下,11.2L酒精含有的分子数为0.5NA |
11.下列关于热化学反应的描述中正确的是( )
| A. | HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热为2×(-57.3)kJ/mol | |
| B. | CO(g)的燃烧热是283.0 kJ/mol,则表示CO燃烧热的热化学方程式为:CO(g)+$\frac{1}{2}$O2(g)═CO2 (g)△H=-283.0 kJ/mol | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 等物质的量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
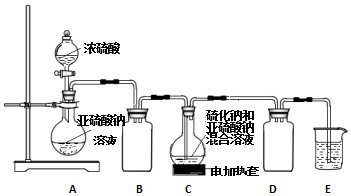
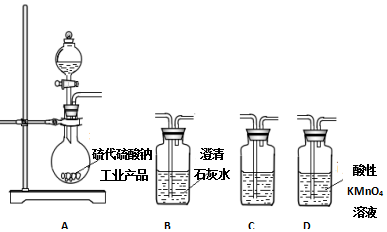
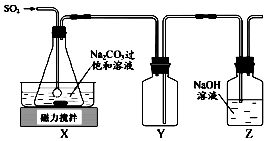 焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中,受热时均易分解.实验室制备少量Na2S2O5的方法:在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2,实验装置如图所示.
焦亚硫酸钠(Na2S2O5)是常用的抗氧化剂,在空气中,受热时均易分解.实验室制备少量Na2S2O5的方法:在不断搅拌下,控制反应温度在40℃左右,向Na2CO3过饱和溶液中通入SO2,实验装置如图所示.