题目内容
下列叙述正确的是( )
①Fe与S混合加热生成FeS2
②澄清石灰水可用来鉴别Na2CO3和NaHCO3溶液
③Na2O2与水反应,红热的Fe与水蒸气反应均能生成碱
④铵盐易分解,均可分解得到NH3
⑤过量的铜与浓硝酸反应可能有一氧化氮生成
⑥浓硫酸可用于干燥H2、Cl2、HBr等气体,但不能干燥NH3、HI.
①Fe与S混合加热生成FeS2
②澄清石灰水可用来鉴别Na2CO3和NaHCO3溶液
③Na2O2与水反应,红热的Fe与水蒸气反应均能生成碱
④铵盐易分解,均可分解得到NH3
⑤过量的铜与浓硝酸反应可能有一氧化氮生成
⑥浓硫酸可用于干燥H2、Cl2、HBr等气体,但不能干燥NH3、HI.
| A、①②④ | B、①②⑤ |
| C、⑤ | D、③⑤⑥ |
考点:钠的重要化合物,铵盐,硝酸的化学性质,铁的化学性质,气体的净化和干燥
专题:
分析:①Fe与S混合加热生成FeS;
②Na2CO3和NaHCO3两种溶液与石灰水反应均生成碳酸钙白色沉淀;
③Na2O2与水反应生成氢氧化钠和氧气,红热的Fe与水蒸气反应生成四氧化三铁和氢气;
④硝酸铵分解不生成氨气;
⑤过量的铜与浓硝酸反应先生成二氧化氮,后有一氧化氮生成;
⑥浓硫酸可用于干燥中性和不具有还原性的气体;
②Na2CO3和NaHCO3两种溶液与石灰水反应均生成碳酸钙白色沉淀;
③Na2O2与水反应生成氢氧化钠和氧气,红热的Fe与水蒸气反应生成四氧化三铁和氢气;
④硝酸铵分解不生成氨气;
⑤过量的铜与浓硝酸反应先生成二氧化氮,后有一氧化氮生成;
⑥浓硫酸可用于干燥中性和不具有还原性的气体;
解答:
解:①S有弱氧化性,S与Fe混合加热生成FeS,故错误;
②Na2CO3和NaHCO3两种溶液与石灰水反应均生成碳酸钙白色沉淀,不能鉴别,应选氯化钙,故错误;
③Na2O2与水反应生成氢氧化钠和氧气,红热的Fe与水蒸气反应生成四氧化三铁和氢气,故错误;
④硝酸铵分解不生成氨气,NH4NO3
N2O↑+2H2O,故错误;
⑤过量的铜与浓硝酸反应先生成二氧化氮,随着反应进行硝酸的浓度减小,稀硝酸与Cu反应生成一氧化氮,故正确;
⑥浓硫酸可用于干燥H2、Cl2、HBr、HI,但不能干燥NH3,氨气是碱性气体,二者之间会发生反应,故错误;
故选C.
②Na2CO3和NaHCO3两种溶液与石灰水反应均生成碳酸钙白色沉淀,不能鉴别,应选氯化钙,故错误;
③Na2O2与水反应生成氢氧化钠和氧气,红热的Fe与水蒸气反应生成四氧化三铁和氢气,故错误;
④硝酸铵分解不生成氨气,NH4NO3
| ||
⑤过量的铜与浓硝酸反应先生成二氧化氮,随着反应进行硝酸的浓度减小,稀硝酸与Cu反应生成一氧化氮,故正确;
⑥浓硫酸可用于干燥H2、Cl2、HBr、HI,但不能干燥NH3,氨气是碱性气体,二者之间会发生反应,故错误;
故选C.
点评:本题考查了元素化合物的有关性质,题目难度不大,注意把握常见元素及其化合物的性质,注意反应物的量不同时产物可能不同.

练习册系列答案
相关题目
 “人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简
“人文奥运”的一个重要体现是:坚决反对运动员服用兴奋剂.某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
| A、遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 |
| B、滴入KMnO4(H+)溶液,观察紫色褪去,能证明结构中存在碳碳双键 |
| C、该分子中的所有碳原子不可能共平面 |
| D、1 mol该物质与浓溴水和H2反应最多消耗Br2和H2分别为4 mol、7 mol |
下列说法中正确的是( )
| A、凡是放热反应都是自发的,吸热反应都是非自发的 |
| B、自发反应一定是△S>0,非自发反应一定是△S<0 |
| C、△S>0且放热的反应一定是自发反应 |
| D、非自发反应在任何条件下都不能实现 |
下列烷烃在光照下与氯气反应,生成一氯代物种类最多的是( )
A、 |
B、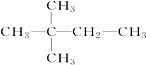 |
| C、CH3CH2CH2CH3 |
D、 |
对铜-锌-稀硫酸组成的原电池装置中,当导线中有1mol电子通过时,理论上的两极变化是:①锌片溶解了32.5g ②锌片增重了32.5g ③铜片上析出1g氢气 ④铜片上析出1mol氢气( )
| A、①③ | B、①④ | C、②③ | D、②④ |
下列实验过程中,溶液始终无明显现象发生的是( )
| A、NO2通入FeSO4溶液中 |
| B、SO2通入酸性KMnO4溶液中 |
| C、NH3通入AlCl3溶液中 |
| D、SO2通入CaCl2溶液中 |
关于卤素(用X表示)的下列叙述中,正确的是( )
| A、卤素单质与水反应均可用X2+H2O═HXO+HX表示 |
| B、HX都极易溶于水,它们的热稳定性随着核电荷数的增加而增强 |
| C、从F2到I2,卤素单质的颜色随着相对分子质量的增大而加深 |
| D、X-离子的还原性F-<Cl-<Br-<I-,因此,相对分子质量小的卤素单质可将相对分子质量大的卤素从它的盐溶液里置换出来 |
下列说法中错误的是( )
| A、化学反应中的能量变化通常表现为热量的变化 |
| B、化学键的断裂和形成是化学反应中能量变化的主要原因 |
| C、断开化学键的过程会放出能量 |
| D、反应物和生成物总能量的相对大小决定了反应是放出能量还是吸收能量 |
下列微粒中:①13Al3+② ③Cl- ④F-,其核外电子数相同的是( )
③Cl- ④F-,其核外电子数相同的是( )
 ③Cl- ④F-,其核外电子数相同的是( )
③Cl- ④F-,其核外电子数相同的是( )| A、①②③ | B、②③④ |
| C、①②④ | D、①②③④ |