题目内容
化学与社会、生活密切相关.下列说法正确的是( )
| A、SO2可用作漂白剂是因为其具有氧化性 |
| B、半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 |
| C、洁厕灵(有效成分为HCl)与84消毒液(有效成分为NaClO)混合使用可增加卫浴的清洁效果 |
| D、高铁酸钾(K2FeO4)是一种高效、多功能水处理剂,既能消毒杀菌又能净水 |
考点:二氧化硫的化学性质,氧化还原反应,氯、溴、碘及其化合物的综合应用,硅的用途
专题:
分析:A.依据二氧化硫漂白的原理解答;
B.二氧化硅为绝缘体;
C.盐酸与次氯酸反应生成氯气;
D.高铁酸钾具有强氧化性,被还原生成Fe3+,Fe3+水解生成氢氧化铁胶体,具有吸附性;
B.二氧化硅为绝缘体;
C.盐酸与次氯酸反应生成氯气;
D.高铁酸钾具有强氧化性,被还原生成Fe3+,Fe3+水解生成氢氧化铁胶体,具有吸附性;
解答:
解:A.二氧化硫能够与有机色素化合生成无色物质而具有漂泊性,故A错误;
B.计算机芯片的材料是硅,不是二氧化硅,故B错误;
C.洁厕灵(有效成分为HCl)与84消毒液(有效成分为NaClO)混合使用发生氧化还原反应生成氯气,容易引起中毒,故C错误;
D.高铁酸钾具有强氧化性,可用于杀菌消毒,被还原生成Fe3+,水解生成氢氧化铁胶体,具有吸附性,可用于净水,故D正确;
故选:D.
B.计算机芯片的材料是硅,不是二氧化硅,故B错误;
C.洁厕灵(有效成分为HCl)与84消毒液(有效成分为NaClO)混合使用发生氧化还原反应生成氯气,容易引起中毒,故C错误;
D.高铁酸钾具有强氧化性,可用于杀菌消毒,被还原生成Fe3+,水解生成氢氧化铁胶体,具有吸附性,可用于净水,故D正确;
故选:D.
点评:本题考查了元素化合物知识,明确二氧化硫、高铁酸钾的性质是解题关键,注意硅与二氧化硅的用途的区别,题目难度不大.

练习册系列答案
相关题目
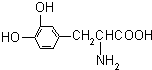 L-多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如图:
L-多巴是一种有机物,它可用于帕金森综合症的治疗,其结构简式如图:这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果.下列关于L-多巴酸碱性的叙述正确的是( )
| A、既没有酸性,又没有碱性 |
| B、既具有酸性,又具有碱性 |
| C、只有酸性,没有碱性 |
| D、只有碱性,没有酸性 |
下列物质中,既能因发生化学反应使溴水褪色,又能使酸性KMnO4溶液褪色的是( )
①SO2②CH3CH2CH=CH2③苯 ④苯酚 ⑤甲苯 ⑥CH3CH3.
①SO2②CH3CH2CH=CH2③苯 ④苯酚 ⑤甲苯 ⑥CH3CH3.
| A、①②③④ | B、全部 |
| C、①②⑤ | D、①②④ |
在水溶液中能大量共存的一组离子是( )
| A、Ag+、Ca2+、Cl-、Br- |
| B、I-、H+、SO42-、ClO- |
| C、Al3+、NH4+、Cl-、CO32- |
| D、K+、Mg2+、NO3-、SCN- |
ClO2是一种杀菌消毒效率高、二次污染小的水处理剂,实验室中可通过以下反应制得:2KClO3+H2C2O4+H2SO4
2ClO2↑+K2SO4+2CO2↑+2H2O据此,下列说法不正确的是( )
| ||
| A、KClO3发生还原反应 |
| B、H2C2O4在反应中被氧化 |
| C、H2C2O4的氧化性强于ClO2的氧化性 |
| D、每1 mol ClO2生成,该反应转移的电子数约为6.02×1023 |
下列有关化学用语能表示甲烷的分子组成,但不能反映其分子空间构型的是( )
A、结构示意图: |
B、电子式: |
C、球棍模型: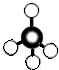 |
D、比例模型: |
 下表各组物质之间通过一步反应不可以实现如图所示转化关系的是( )
下表各组物质之间通过一步反应不可以实现如图所示转化关系的是( )