题目内容
写出下列化学反应的离子方程式.
(1)盐酸与NaOH溶液反应 .
(2)锌和稀硫酸反应 .
(3)CaO与稀盐酸反应 .
(4)CuSO4溶液与Ba(OH)2溶液反应 .
(1)盐酸与NaOH溶液反应
(2)锌和稀硫酸反应
(3)CaO与稀盐酸反应
(4)CuSO4溶液与Ba(OH)2溶液反应
考点:离子方程式的书写
专题:
分析:(1)盐酸与NaOH溶液反应生成氯化钠和水;
(2)锌和稀硫酸反应生成硫酸锌和氢气;
(3)CaO与稀盐酸反应生成氯化钙和水;
(4)CuSO4溶液与Ba(OH)2溶液反应生成硫酸钡和氢氧化铜沉淀.
(2)锌和稀硫酸反应生成硫酸锌和氢气;
(3)CaO与稀盐酸反应生成氯化钙和水;
(4)CuSO4溶液与Ba(OH)2溶液反应生成硫酸钡和氢氧化铜沉淀.
解答:
解:(1)盐酸与NaOH溶液反应生成氯化钠和水,离子方程式为:H++OH-=H2O;
故答案为:H++OH-=H2O;
(2)锌和稀硫酸反应生成硫酸锌和氢气,离子方程式:Zn+2H+=H2↑+Zn2+;
故答案为:Zn+2H+=H2↑+Zn2+;
(3)CaO与稀盐酸反应生成氯化钙和水,离子方程式为:CaO+2H+=H2O+Ca2+;
故答案为:CaO+2H+=H2O+Ca2+;
(4)CuSO4溶液与Ba(OH)2溶液反应生成硫酸钡和氢氧化铜沉淀,离子方程式为:Cu2++SO42-+Ba2++2 OH-=Cu(OH)2↓+BaSO4↓;
故答案为:Cu2++SO42-+Ba2++2 OH-=Cu(OH)2↓+BaSO4↓.
故答案为:H++OH-=H2O;
(2)锌和稀硫酸反应生成硫酸锌和氢气,离子方程式:Zn+2H+=H2↑+Zn2+;
故答案为:Zn+2H+=H2↑+Zn2+;
(3)CaO与稀盐酸反应生成氯化钙和水,离子方程式为:CaO+2H+=H2O+Ca2+;
故答案为:CaO+2H+=H2O+Ca2+;
(4)CuSO4溶液与Ba(OH)2溶液反应生成硫酸钡和氢氧化铜沉淀,离子方程式为:Cu2++SO42-+Ba2++2 OH-=Cu(OH)2↓+BaSO4↓;
故答案为:Cu2++SO42-+Ba2++2 OH-=Cu(OH)2↓+BaSO4↓.
点评:本题为离子方程式书写的考查,题目难度不大,明确反应的实质,注意化学式的拆分、原子个数守恒、电荷数守恒即可解答本题,侧重对基础在知识的考查.

练习册系列答案
 启东小题作业本系列答案
启东小题作业本系列答案
相关题目
下列各组物质,属于电解质是( )
| A、熔融NaCl | B、铜 |
| C、酒精 | D、硫酸溶液 |
下列关于
Ne和
Ne的说法正确的是( )
| ||
| 10 |
| ||
| 10 |
| A、质子数相等 | B、质量数相等 |
| C、中子数相等 | D、性质相同 |
下列叙述正确的是( )
| A、电解NaCl溶液时,阴极产生1 mol Cl2的同时阳极产生l molH2 |
| B、0.1 mol?L-1AlCl3溶液中Al3+的浓度为0.1 mol?L-1 |
| C、7 g 14C中所含中子数为4 NA(设NA为阿伏加德罗常数的值) |
| D、2.24 L氯气与足量NaOH稀溶液反应,转移0.1 mol电子 |
下列说法正确的是( )
| A、氮原子的质量就是氮的相对原子质量 |
| B、氢氧化钠的摩尔质量是40 g |
| C、1 mol H2SO4中含有1 mol H2 |
| D、氩气的摩尔质量在数值上等于它的相对原子质量 |
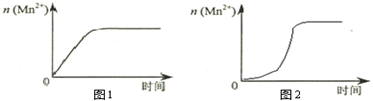
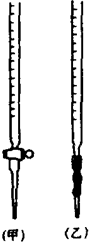 某化学兴趣小组为了测定草酸浓度及硫酸酸化的高锰酸钾溶液与草酸(H2C2O4)溶液反应的化学反应速率大小并验证离子反应的本质,设计了如下实验.化学反应如下:KMnO4+H2C2O4+H2SO4-K2SO4+MnSO4+CO2↑+H2O 实验主要步骤如下:Ⅰ.用0.1000mol?L-1酸性高锰酸钾溶液滴定未知浓度的H2C2O4溶液Ⅱ.测定化学反应速率.Ⅲ.验证紫红色是MnO4-离子.请回答:
某化学兴趣小组为了测定草酸浓度及硫酸酸化的高锰酸钾溶液与草酸(H2C2O4)溶液反应的化学反应速率大小并验证离子反应的本质,设计了如下实验.化学反应如下:KMnO4+H2C2O4+H2SO4-K2SO4+MnSO4+CO2↑+H2O 实验主要步骤如下:Ⅰ.用0.1000mol?L-1酸性高锰酸钾溶液滴定未知浓度的H2C2O4溶液Ⅱ.测定化学反应速率.Ⅲ.验证紫红色是MnO4-离子.请回答: