题目内容
8.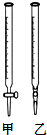 NaH2PO4、Na2HPO4可用于合成化工原料三聚磷酸钠(Na5P3O10).
NaH2PO4、Na2HPO4可用于合成化工原料三聚磷酸钠(Na5P3O10).(1)能说明NaH2PO4溶液显弱酸性原因的离子方程式为H2PO4-?HPO42-+H+.
(2)能说明Na2HPO4溶液显弱碱性原因的离子方程式为HPO42-+H2O?H2PO4-+OH-.
(3)测定某三聚磷酸钠试样中Na5P3O10的含量可用间接滴定法,其流程如下:
样品1.3000g$\stackrel{稀硝酸}{→}$H3PO4$→_{调pH到3-4}^{用NaOH(aq)}$NaH2PO4→$\stackrel{配成100.00mL}{溶液A}$$\stackrel{取样}{→}$$→_{指示剂X}^{0.1000mol.L-1NaOH溶液滴}$Na2HPO4
1滴定时所用的指示剂X可为酚酞.
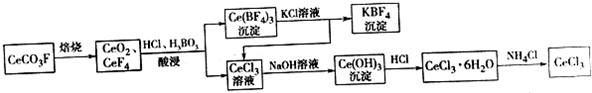
②NaOH标准溶液应盛放在如图所示的滴定管乙(选填:“甲”或“乙”) 中.
③滴定实验记录如下表(样品中杂质不与酸或碱反应).
| 滴定次数 | 待测溶液A的体积(/mL) | 0.1000mol•L-1NaOH溶液的体积 | |
| 滴定前读数(/mL) | 滴定后读数(/mL) | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 21.99 |
| 3 | 25.00 | 0.20 | 20.20 |
分析 (1)NaH2PO4溶液显弱酸性,说明H2PO4-在水溶液里电离程度大于水解程度;
(2)Na2HPO4溶液显弱碱性,说明HPO42-的水解程度大于电离程度;
(3)①NaH2PO4溶液显弱酸性,应该用酚酞作指示剂;
②碱只能用碱式滴定管量取;
③A中成分是NaH2PO4,能和氢氧化钠反应生成Na3PO4,反应方程式为NaH2PO4+NaOH=Na3PO4+H2O,氢氧化钠的平均体积=$\frac{(21.03-1.02)+(21.99-2.00)+(20.20-0.20)}{3}$mL=20.00mL,根据方程式计算A的物质的量浓度,再根据P原子守恒计算Na5P3O10的质量分数.
解答 解:(1)NaH2PO4溶液显弱酸性,说明H2PO4-在水溶液里电离程度大于水解程度,该阴离子电离方程式为H2PO4-?HPO42-+H+,
故答案为:H2PO4-?HPO42-+H+;
(2)Na2HPO4溶液显弱碱性,说明HPO42-的水解程度大于电离程度,该阴离子水解方程式为HPO42-+H2O?H2PO4-+OH-,
故答案为:HPO42-+H2O?H2PO4-+OH-;
(3)①NaH2PO4溶液显弱酸性,应该用酚酞作指示剂,滴定终点时颜色变化明显,故答案为:酚酞;
②氢氧化钠溶液呈碱性,应该用碱式滴定管乙盛放,故选乙;
③A中成分是NaH2PO4,能和氢氧化钠反应生成Na3PO4,反应方程式为NaH2PO4+NaOH=Na2HP4+H2O,氢氧化钠的平均体积=$\frac{(21.03-1.02)+(21.99-2.00)+(20.20-0.20)}{3}$mL=20.00mL,根据方程式得c(A)=$\frac{0.1000mol/L×0.02000L}{0.02500L}$=0.0800mol/L,100mL溶液中n(A)=0.008mol,根据P原子守恒得m(Na5P3O10)=0.008mol÷3×368g/mol=0.9813g,质量分数=$\frac{0.9813g}{1.3000g}×100%$=75.5%,
故答案为:75.5%.
点评 本题考查了物质含量的测定及物质的性质,根据物质之间的反应结合原子守恒计算物质含量,计算量较大,注意小数的保留,难度中等.

| A. | 熔融的KOH | B. | KOH溶液 | C. | 浓硫酸 | D. | KOH晶体 |
| A. | 等体积、等物质的量浓度的氨水与盐酸混合 | |
| B. | 常温下,pH=8的氨水与pH=6的硝酸等体积混合 | |
| C. | 常温下,pH=12的Ba(OH)2溶液与pH=2的NaHSO4溶液等体积混合 | |
| D. | c(H+)=c(OH-)=10-6 mol•L-1的溶液 |
| A. | 向AgI中加一定浓度、一定体积的NaCl溶液,AgI可转化为AgCl | |
| B. | 常温下,AgCl若要在NaI溶液中开始转化为AgI,则NaI的浓度应该大于$\frac{1}{\sqrt{1.8}}$×10-11mol/L | |
| C. | AgI比AgCl更难溶于水,AgCl可以转化为AgI | |
| D. | 向c(Ag+)=1.8×10-4mol/L的溶液中加入等体积NaCl溶液,开始出现AgCl沉淀,则NaCl溶液浓度应大于1.0×10-6mol/L |
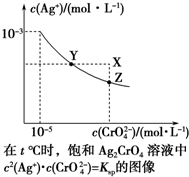 已知t℃时AgCl的Ksp=4×10-10,在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法错误的是( )
已知t℃时AgCl的Ksp=4×10-10,在t℃时,Ag2CrO4在水中的沉淀溶解平衡曲线如图所示.下列说法错误的是( )| A. | 在t℃时,Ag2CrO4的Ksp为1×10-11 | |
| B. | 在饱和溶液中加入K2CrO4(s)可使溶液由Y点到Z点 | |
| C. | 在t℃,Ag2CrO4(s)+2Cl-(aq)?2AgCl(s)+CrO${\;}_{4}^{2-}$(aq)平衡常数K=6.25×107 | |
| D. | 在t℃时,以0.001 mol•L-1 AgNO3溶液滴定20 mL 0.001 mol•L-1 KCl和0.001 mol•L-1的K2CrO4的混合溶液,CrO${\;}_{4}^{2-}$先沉淀 |
| A. | 向饱和AgCl水溶液中加入少量的NaCl固体,Ksp(AgCl)变大 | |
| B. | AgNO3溶液与NaCl溶液混合后的溶液中,一定有c(Ag+)=c(Cl-) | |
| C. | 25℃时,当溶液中c(Ag+)×c(Cl-)=Ksp(AgCl)时,此溶液为AgCl的饱和溶液 | |
| D. | 将固体AgCl加入到浓KI溶液中,部分AgCl转化为AgI,故AgCl溶解度小于AgI |
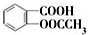 )是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128℃~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐为主要原料合成阿司匹林,反应原理如下:
)是世界上应用最广泛的解热、镇痛和抗炎药.乙酰水杨酸受热易分解,分解温度为128℃~135℃.某学习小组在实验室以水杨酸(邻羟基苯甲酸)与醋酸酐为主要原料合成阿司匹林,反应原理如下: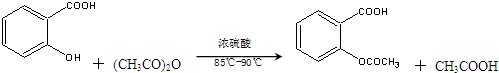
制备基本操作流程如下:
醋酸酐+水杨酸$\stackrel{浓硫酸}{→}$$\stackrel{摇匀}{→}$$\stackrel{85℃-90℃加热}{→}$$\stackrel{冷却}{→}$$→_{洗涤}^{减压过滤}$粗产品
主要试剂和产品的物理常数如下表所示:
| 名称 | 相对分子质量 | 熔点或沸点(℃) | 水溶性 |
| 水杨酸 | 138 | 158(熔点) | 微溶 |
| 醋酸酐 | 102 | 139.4(沸点) | 易水解 |
| 乙酰水杨酸 | 180 | 135(熔点) | 微溶 |
(1)制备阿司匹林时,要使用干燥的仪器的原因是醋酸酐和水易发生反应.
(2)合成阿司匹林时,最合适的加热方法是水浴加热.
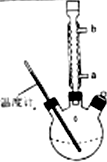
(3)提纯粗产品流程如下,加热回流装置如图:
粗产品$→_{沸石}^{乙酸乙酯}$$→_{回流}^{加热}$$\stackrel{趁热过滤}{→}$$→_{减压过滤}^{冷却}$$→_{干燥}^{洗涤}$乙酰水杨酸
①使用温度计的目的是控制加热的温度,防止乙酰水杨酸受热易分解.
②冷凝水的流进方向是a(填“a”或“b”);
③趁热过滤的原因是防止乙酰水杨酸结晶析出.
④下列说法正确的是abc(填选项字母).
a.此种提纯方法中乙酸乙酯的作用是做溶剂
b.此种提纯粗产品的方法叫重结晶
c.根据以上提纯过程可以得出阿司匹林在乙酸乙酯中的溶解度低温时大
d.可以用紫色石蕊溶液判断产品中是否含有未反应完的水杨酸
(4)在实验中原料用量:2.0g水杨酸、5.0mL醋酸酐(ρ=1.08/cm3),最终称得产品质量为2.2g,则所得乙酰水杨酸的产率为84.3%(用百分数表示,小数点后一位).