题目内容
12.取物质的量浓度相等的CuCl2、FeCl3的混合溶液40mL平分于两只试管,向其中一只试管加入足量AgNO3溶液生成14.35g 沉淀,向另一只试管加入1.12g 还原铁粉充分反应后该试管溶液中存在的金属阳离子及其物质的量浓度是( )| A. | Fe2+ 2mol/L、Cu2+ 0.5mol/L | B. | Fe2+ 1mol/L、Fe3+ 1mol/L | ||
| C. | Fe2+ 0.5mol/L、Cu2+ 0.25mol/L | D. | Fe2+ 1.5mol/L、Cu2+ 0.5mol/L |
分析 14.35g沉淀为氯化银,其物质的量为:$\frac{14.35g}{143.5g/mol}$=0.1mol,说明每份溶液中含有0.1mol氯离子,每份溶液中氯离子的浓度为:$\frac{0.1mol}{0.02L}$=5mol/L;1.12gFe的物质的量为:$\frac{1.12g}{56g/mol}$=0.02mol,向另一只试管中加入0.02molFe后,阴离子的浓度不变,仍然为5mol/L,则阳离子的总电荷浓度一定为5mol/L,然后结合反应先后顺序对各选项进行判断.
解答 解:14.35g沉淀为氯化银,其物质的量为:$\frac{14.35g}{143.5g/mol}$=0.1mol,说明每份溶液中含有0.1mol氯离子,每份溶液中氯离子的浓度为:$\frac{0.1mol}{0.02L}$=5mol/L,
1.12gFe的物质的量为:$\frac{1.12g}{56g/mol}$=0.02mol,向另一只试管中加入0.02molFe后,阴离子的浓度不变,仍然为5mol/L,则阳离子的总电荷浓度一定为5mol/L,
A.Fe2+2mol/L、Cu2+0.5mol/L,则阳离子总电荷浓度为:2mo/L×2+0.5mol/L×2=5mol/L,满足条件,故A正确;
B.Fe2+ 1mol/L、Fe3+ 1mol/L;若反应后存在Fe3+,由于Fe3+优先与Fe反应,则溶液中的阳离子一定还存在Cu2+,故B错误;
C.Fe2+ 0.5mol/L、Cu2+ 0.25mol/L,阳离子总浓度为:0.5mol/L×2+0.25mol/L×2=1.5mol/L,不满足条件,故C错误;
D.Fe2+ 1.5mol/L、Cu2+ 0.5mol/L,阳离子总浓度为:1.5mol/L×2+0.5mol/L×2=4mol/L,不满足条件,故D错误;
故选A.
点评 本题考查了物质的量浓度的计算,题目难度中等,明确发生反应的先后顺序为解答关键,注意掌握守恒思想在化学计算中的应用,试题培养了学生的化学计算能力.

| A. | 再加点溶质到容量瓶中去 | B. | 影响不大,不再处理 | ||
| C. | 用胶头滴管准确吸出标线上的溶液 | D. | 重新配制 |
| A. | 1:4 | B. | 1:3 | C. | 1:2 | D. | 1:1 |
| A. | 萃取操作时,可以选用CCl4或酒精作为萃取剂从碘水中萃取碘 | |
| B. | 蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热 | |
| C. | 分液操作时,下层液体从分液漏斗下口放出,上层液体从下口放出到另一个烧杯中 | |
| D. | 蒸馏操作时,收集完馏分后,先停止加热,待恢复室温后再停止通冷凝水 |
| A. | NH4+、Cu2+、Cl-、NO3- | B. | Fe2+、Na+、NO3-、Cl- | ||
| C. | K+、Na+、CO32-、SO42- | D. | K+、Na+、SO42-、S2- |
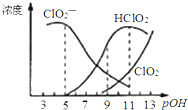 亚氯酸钠(NaClO2)用于漂白织物、纤维、纸浆,具有对纤维损伤小的特点.其在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用.已知pOH=-lgc(OH-),经测定25℃时各组分含量随pOH变化情况如图所示(Cl-没有画出),此温度下,下列分析错误的是( )
亚氯酸钠(NaClO2)用于漂白织物、纤维、纸浆,具有对纤维损伤小的特点.其在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用.已知pOH=-lgc(OH-),经测定25℃时各组分含量随pOH变化情况如图所示(Cl-没有画出),此温度下,下列分析错误的是( )| A. | HClO2的电离平衡常数的数值Ka=10-6 | |
| B. | 亚氯酸钠在碱性条件下较稳定 | |
| C. | pH=7时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2-)>c( ClO2)>c( Cl-) | |
| D. | 同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有c(HClO2)+2c(H+)=c(ClO2-)+2c(OH-) |
| A. | 向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| B. | NH4HCO3溶液与过量KOH浓溶液共热:NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| C. | 氢氧化钙溶液与碳酸氢镁溶液反应:Ca2++OH-+HCO3-═CaCO3↓+H2O | |
| D. | KI溶液与H2SO4酸化的H2O2溶液混合:2 I-+H2O2+2 H+═2 H2O+I2 |