题目内容
 短周期元素A、B、C、D、F原子序数依次增大.A是周期表中原子半径最小的元素,B是形成化合物种类最多的元素,C是自然界含量最多的元素,D是同周期中金属性最强的元素,F的负一价离子与C的某种氢化物分子含有相同的电子数.
短周期元素A、B、C、D、F原子序数依次增大.A是周期表中原子半径最小的元素,B是形成化合物种类最多的元素,C是自然界含量最多的元素,D是同周期中金属性最强的元素,F的负一价离子与C的某种氢化物分子含有相同的电子数.(1)A、C、D形成的化合物中含有的化学键类型为
(2)已知:①F-F→2F;△H=+a kJ?mol-1
②2A→A-A;△H=-b kJ?mol-1
③F+A→AF;△H=-c kJ?mol-1
写出298K时,A2与F2反应的热化学方程式
(3)在某温度下、容积均为2L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g)?X(g);△H=-aJ?mol-1(a>0,X为A、B、C三种元素组成的一种化合物).初始投料与各容器达到平衡时的有关数据如下:
| 容 器 | 甲 | 乙 | 丙 |
| 初始投料 | 2molA2、1molBC | 1molX | 4molA2、2molBC |
| 平衡时n(X) | 0.5mol | n2 | n3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 体系的压强 | P1 | P2 | P3 |
| 反应物的转化率 | α1 | α2 | α3 |
②该温度下,反应2A2(g)+BC(g)?X(g) 的平衡常数K值为
③三个容器中的反应分别达平衡时各组数据关系正确的是
A.α1+α2=1 B.Q1+Q2=a C.α3<α1
D.P3<2P1=2P2 E.n2<n3<1.0mol F.Q3=2Q1
④在其他条件不变的情况下,将甲容器的体系体积压缩到1L,若在第8min达到新的平衡时A2的总转化率为75%,请在如图中画出第5min 到新平衡时X的物质的量浓度的变化曲线.
考点:化学平衡的计算,用盖斯定律进行有关反应热的计算,物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:A是周期表中原子半径最小的元素,即为H,B是形成化合物种类最多的元素,即为C,C是自然界含量最多的元素,即为O,D是同周期中金属性最强的元素,即为Na,F的负一价离子与C的氢化物分子含有相同的电子数,即为Cl.
(1)氢氧化钠中的成键情况确定化学键组成;
(2)根据热化学方程式的书写方法结合盖斯定律来计算;
(3)①根据v=
来计算化学反应速率;
②用三行式计算化学平衡常数;
③根据等效平衡知识借助极限转化思想来回答判断;
④根已知条件求出甲醇在5min和8min时的物质的量浓度,然后再作图即可.
(1)氢氧化钠中的成键情况确定化学键组成;
(2)根据热化学方程式的书写方法结合盖斯定律来计算;
(3)①根据v=
| △c |
| △t |
②用三行式计算化学平衡常数;
③根据等效平衡知识借助极限转化思想来回答判断;
④根已知条件求出甲醇在5min和8min时的物质的量浓度,然后再作图即可.
解答:
解:A是周期表中原子半径最小的元素,即为H,B是形成化合物种类最多的元素,即为C,C是自然界含量最多的元素,即为O,D是同周期中金属性最强的元素,即为Na,F的负一价离子与C的氢化物分子含有相同的电子数,
即为Cl.
(1)A、C、D形成的化合物中含有的化学键类型为:离子键、共价键,故答案为:离子键、共价键;
(2)已知①Cl-Cl→2Cl;△H=+a kJ?mol-1
②2H→H-H;△H=-b kJ?mol-1
③Cl+H→HCl;△H=-c kJ?mol-1
所以H2(g)+Cl2(g)=2HCl(g)可以是①-②+③×2得到的,所以反应的焓变△H=-(2c-a-b)kJ/mol,故答案为:H2(g)+Cl2(g)=2HCl(g)△H=-(2c-a-b)kJ/mol;
(3)①2H2(g)+CO(g)?CH3OH(g);
初始量:2 1 0
变化量:1 0.5 0.5
平衡量:1 0.5 0.5
在该温度下,A2的平均反应速率v( A2)=
=0.125 mol?L-1?min-1,故答案为:0.125 mol?L-1?min-1;
②该温度下,反应2A2(g)+BC(g)?X(g) 的平衡常数K=
=4mol-2?L2,故答案为:4mol-2?L2;
③A、投料2molH2、1molCO和1molCH4O建立的平衡是等效的,只是建立的方向不一样,所以α1+α2=1,故A正确;
B、料2molH2、1molCO和1molCH3OH建立的平衡是等效的,反应2H2(g)+CO(g)?CH3OH(g)是放热的,放出的热量应该是Q1+Q2=a,故B正确;
C、当氢气和一氧化碳的投料增加一倍,则压强会增大,导致化学平衡正向移动,移动的结果是反应物的转化率增大,即α3>α1,故C错误;
D、投料2molH2、1molCO和1molCH3OH建立的平衡是等效的,所以P1=P2,当氢气和一氧化碳的投料增加一倍,则压强应是增大一倍,但是压强增大,导致化学平衡正向移动,移动的结果是压强比原来的2倍要小,即P3<2P1=2P2,故D正确;
E、当氢气和一氧化碳的投料增加一倍,能量变化数值理论上也应该是原来的2倍,但是压强引起化学平衡正向,而正向放热,结果使得Q3>2Q1,故E错误.
选ABD.
④将甲容器的体系体积压缩到1L,若在第8min 达到新的平衡时,
2H2(g)+CO(g)?CH4O(g)
初始量:2 1 0
变化量:1.5 0.75 0.75
平衡量:0.5 0.25 0.75
所以达到平衡时,甲醇的物质的量浓度是0.75mol/L,在第5min时,由于体积减半,所以甲醇的浓度应该加倍,即为0.25mol/L×2=0.5mol/L,所以5-8min内,甲醇的物质的量浓度从0.5mol/L升高到0.75mol/L,如图所示: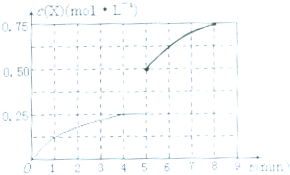
,故答案为:
.
即为Cl.
(1)A、C、D形成的化合物中含有的化学键类型为:离子键、共价键,故答案为:离子键、共价键;
(2)已知①Cl-Cl→2Cl;△H=+a kJ?mol-1
②2H→H-H;△H=-b kJ?mol-1
③Cl+H→HCl;△H=-c kJ?mol-1
所以H2(g)+Cl2(g)=2HCl(g)可以是①-②+③×2得到的,所以反应的焓变△H=-(2c-a-b)kJ/mol,故答案为:H2(g)+Cl2(g)=2HCl(g)△H=-(2c-a-b)kJ/mol;
(3)①2H2(g)+CO(g)?CH3OH(g);
初始量:2 1 0
变化量:1 0.5 0.5
平衡量:1 0.5 0.5
在该温度下,A2的平均反应速率v( A2)=
| ||
| 4min |
②该温度下,反应2A2(g)+BC(g)?X(g) 的平衡常数K=
| ||||
(
|
③A、投料2molH2、1molCO和1molCH4O建立的平衡是等效的,只是建立的方向不一样,所以α1+α2=1,故A正确;
B、料2molH2、1molCO和1molCH3OH建立的平衡是等效的,反应2H2(g)+CO(g)?CH3OH(g)是放热的,放出的热量应该是Q1+Q2=a,故B正确;
C、当氢气和一氧化碳的投料增加一倍,则压强会增大,导致化学平衡正向移动,移动的结果是反应物的转化率增大,即α3>α1,故C错误;
D、投料2molH2、1molCO和1molCH3OH建立的平衡是等效的,所以P1=P2,当氢气和一氧化碳的投料增加一倍,则压强应是增大一倍,但是压强增大,导致化学平衡正向移动,移动的结果是压强比原来的2倍要小,即P3<2P1=2P2,故D正确;
E、当氢气和一氧化碳的投料增加一倍,能量变化数值理论上也应该是原来的2倍,但是压强引起化学平衡正向,而正向放热,结果使得Q3>2Q1,故E错误.
选ABD.
④将甲容器的体系体积压缩到1L,若在第8min 达到新的平衡时,
2H2(g)+CO(g)?CH4O(g)
初始量:2 1 0
变化量:1.5 0.75 0.75
平衡量:0.5 0.25 0.75
所以达到平衡时,甲醇的物质的量浓度是0.75mol/L,在第5min时,由于体积减半,所以甲醇的浓度应该加倍,即为0.25mol/L×2=0.5mol/L,所以5-8min内,甲醇的物质的量浓度从0.5mol/L升高到0.75mol/L,如图所示:

,故答案为:

.
点评:本题涉及化学平衡的建立、等效平衡以及化学平衡的有关计算等知识,属于综合知识的考查,难度大,要求学生具有分析和解决问题的能力.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
关于钠原子和钠离子,下列叙述的正确是( )
| A、它们的化学性质相似 |
| B、它们电子层数相同 |
| C、钠原子半径比钠离子半径小 |
| D、钠原子、钠离子均为同一元素 |
同分异构体指的是相同分子式不同分子结构的化合物,它描述的对象主体是化合物.同素异形体、同位素、同系物描述的对象主体依次为( )
| A、单质、原子、化合物 |
| B、元素、单质、化合物 |
| C、无机化合物、元素、有机化合物 |
| D、原子核、原子、分子 |
NA表示阿伏伽德罗常数.下列判断正确的是( )
| A、25℃,pH=13的NaOH溶液中含有OH-的数目为0.1NA |
| B、分别为7.8g的Na2S和Na2O2中含有的阴离子数分别是0.1NA和0.2NA |
| C、常温常压下,22.4L CO2中含有的CO2分子数小于NA个 |
| D、1L 0.1mol/L的氨水含有0.1NA个NH3?H2O |
下列有关说法中,不正确的是( )
| A、a mol/L的HCN溶液与b mol/L的NaOH溶液等体积混合,所得溶液中c(Na+)>c(CN-),则a一定小于b |
| B、常温,CH3COONa溶液的pH=8,则c(Na+)-c(CH3COO-)=9.9×10-7mol/L |
| C、常温下,0.1mol/L的某酸溶液中,若c(OH-)/c(H+)=1×10-8,则溶液中由水电离出的c(H+)=1×10-11mol/L |
| D、在0.1mol/L的Na2SO3溶液中加入少量NaOH固体,c(SO32-)与c(Na+)均增大 |
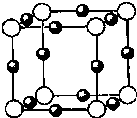 【化学--选修3:物质结构与性质】
【化学--选修3:物质结构与性质】 已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入足量的氯气,二者恰好完全反应.生成Cl-、ClO-、ClO3-三种含氯元素的离子,其中ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示.
已知Ca(OH)2与Cl2反应的氧化产物与温度有关,在一定量的石灰乳中通入足量的氯气,二者恰好完全反应.生成Cl-、ClO-、ClO3-三种含氯元素的离子,其中ClO-、ClO3-两种离子的物质的量(n)与反应时间(t)的曲线如图所示. A、B、C、D是短周期元素形成的四种气体单质.E、F均为气体,且F为红棕色.有关的转化关系如下图所示(反应条件均已略去).请回答下列问题:
A、B、C、D是短周期元素形成的四种气体单质.E、F均为气体,且F为红棕色.有关的转化关系如下图所示(反应条件均已略去).请回答下列问题: