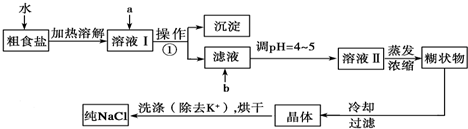
题目内容
对于常温下pH为4的氯化铵溶液与醋酸溶液,下列叙述正确的是( )
| A、溶液中c(H+)相等 |
| B、水电离的c(H+)相等 |
| C、两溶液中水的电离程度相等 |
| D、醋酸溶液中水电离的c(H+)多 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:常温下,氯化铵和醋酸溶液中c(H+)=10-pH,酸或碱抑制水电离,含有弱离子的盐促进水电离,据此分析解答.
解答:
解:A.常温下,氯化铵和醋酸溶液中c(H+)=10-pH,二者的pH相等,所以两种溶液中c(H+)相等,故A正确;
B.氯化铵是强酸弱碱盐,促进水电离,醋酸是弱酸,抑制水电离,所以氯化铵溶液中c(H+)大,故B错误;
C.氯化铵是强酸弱碱盐,促进水电离,醋酸是弱酸,抑制水电离,所以两种溶液中水的电离程度不同,故C错误;
D.氯化铵是强酸弱碱盐,促进水电离,醋酸是弱酸,抑制水电离,所以醋酸溶液中水电离出c(H+)小,故D错误;
故选A.
B.氯化铵是强酸弱碱盐,促进水电离,醋酸是弱酸,抑制水电离,所以氯化铵溶液中c(H+)大,故B错误;
C.氯化铵是强酸弱碱盐,促进水电离,醋酸是弱酸,抑制水电离,所以两种溶液中水的电离程度不同,故C错误;
D.氯化铵是强酸弱碱盐,促进水电离,醋酸是弱酸,抑制水电离,所以醋酸溶液中水电离出c(H+)小,故D错误;
故选A.
点评:本题考查盐类水解和弱电解质的电离,根据溶质的性质确定溶液中水的电离,会计算酸溶液中水电离出c(H+)大小,为易错点.

练习册系列答案
相关题目
短周期元素M、W、X、Y、Z的原子序数依次增大,且M、W、X、Y+、Z2-的电子数与其电子层数的比值依次为1、3、4、5、6(不考虑零族元素).下列关于这些元素的叙述正确的是( )
| A、X分别和其它四种元素均可形成至少2种化合物 |
| B、X、Y、Z离子半径依次增大 |
| C、M、X、Z三种元素组成的化合物含有离子键 |
| D、W、X、Z对应气态氢化物稳定性依次增强 |
CuSO4是一种重要的化工原料,其有关制备途径及性质如图所示.下列说法正确的是( )
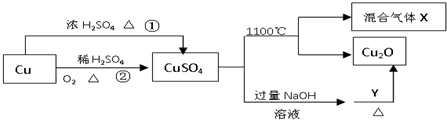

| A、相对于途径①,途径②更好地体现了绿色化学思想 |
| B、Y可以是蔗糖溶液 |
| C、CuSO4在1100℃分解所得气体X可能是SO2和SO3的混合气体 |
| D、将CuSO4溶液蒸发、利用余热蒸干,可制得胆矾晶体 |
 图中X、Y分别是直流电源的两极,通电后,发现a极板质量增加,b极板处有无色无臭气体放出,符合这一情况的是( )
图中X、Y分别是直流电源的两极,通电后,发现a极板质量增加,b极板处有无色无臭气体放出,符合这一情况的是( )| a极板 | b极板 | X电极 | Z溶液 | |
| A | 银 | 铁 | 正极 | AgNO3 |
| B | 石墨 | 石墨 | 负极 | NaOH |
| C | 锌 | 石墨 | 负极 | CuSO4 |
| D | 铜 | 石墨 | 负极 | CuCl2 |
| A、A |
| B、B |
| C、C |
| D、D |
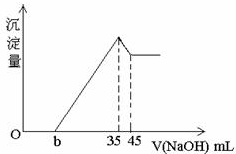 取一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有100mlH2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积关系如图所示.则原H2SO4物质的量溶度是( )
取一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有100mlH2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积关系如图所示.则原H2SO4物质的量溶度是( )| A、A、1mol/L |
| B、B、1.75mol/L |
| C、C、3.5mol/L |
| D、D、2mol/L |
在某一溶液中可能含有下列几种离子:K+、Fe3+、Ag+、Ba2+、NO2-、AlO2-、CO32-、SO32-、SO42-.某该溶液进行有关实验,实验步骤及结果如下:
①向溶液中加入过量稀盐酸,得到气体甲和溶液甲;
②向溶液甲中加入过量NH4HCO3溶液,得到白色沉淀乙、气体乙和溶液乙;
③向溶液乙中加入过量Ba(OH)2溶液并加热,得到白色沉淀丙、气体丙和溶液丙.
④检验气体甲、气体乙、气体丙,都只含有一种成分,而且各不相同.
下列说法正确的是( )
①向溶液中加入过量稀盐酸,得到气体甲和溶液甲;
②向溶液甲中加入过量NH4HCO3溶液,得到白色沉淀乙、气体乙和溶液乙;
③向溶液乙中加入过量Ba(OH)2溶液并加热,得到白色沉淀丙、气体丙和溶液丙.
④检验气体甲、气体乙、气体丙,都只含有一种成分,而且各不相同.
下列说法正确的是( )
| A、气体甲可能为CO2 或者SO2 |
| B、沉淀丙中一定含有BaCO3,可能含有BaSO4 |
| C、该溶液中肯定存在的离子有K+、AlO2-、SO32-、SO42-、NO2- |
| D、只根据实验①能得出溶液中一定没有Fe3+、Ag+、Ba2+,K+是否存在无法确定 |
下列叙述正确的是( )
| A、将一小块铜片放入盛有浓硫酸的试管中加热反应后的溶液呈蓝色 |
| B、将一小块钠放入盛有水的烧杯中,钠在水面上游动,同时看到烧杯内的溶液变为红色 |
C、 如图,一段时间后给烧杯内的溶液中加入黄色的K3[Fe(CN)6]溶液,可看到Fe电极附近有蓝色沉淀生成 |
| D、向盛有少量Mg(OH)2沉淀悬浊液的试管中滴加氯化铵溶液,可看到沉淀溶解 |