题目内容
14.将3.48g四氧化三铁完全溶解在100mL 1mol•L-1硫酸中,然后加K2Cr2O7溶液25mL,恰好使溶液中Fe2+全部转为Fe3+,Cr2O${\;}_{7}^{2-}$全部转化为Cr3+,则K2Cr2O7溶液物质的量浓度是( )| A. | 0.05 mol•L-1 | B. | 0.1 mol•L-1 | C. | 0.2 mol•L-1 | D. | 0.3 mol•L-1 |
分析 四氧化三铁中+2铁占$\frac{1}{3}$,3.48g四氧化三铁为0.015mol,完全溶解后溶液中含有Fe2+为0.015mol,入K2Cr2O7溶液25ml,恰好使溶液中的Fe2+全部转化为Fe3+,Cr2O72-全部转化成Cr3+,根据电子转移守恒计算K2Cr2O7的物质的量,进而计算K2Cr2O7溶液物质的量浓度.
解答 解:3.48g四氧化三铁物质的量为$\frac{3.48g}{232g/mol}$=0.015mol,
四氧化三铁中+2铁占$\frac{1}{3}$,所以完全溶解后溶液中含有Fe2+为0.015mol×3×$\frac{1}{3}$=0.015mol,
加入K2Cr2O7溶液25ml,恰好使溶液中的Fe2+全部转化为Fe3+,Cr2O72-全部转化成Cr3+,根据电子转移守恒:n(Cr2O72-)×2×(6-3)=0.015mol×(3-2),解得n(Cr2O72-)=0.0025mol,
故K2Cr2O7溶液物质的量浓度是$\frac{0.0025mol}{0.025L}$=0.1mol/L,
故选B.
点评 本题考查氧化还原反应的计算,侧重于学生的分析计算能力的考查,涉及两步反应,利用方程式计算比较麻烦,关键抓住氧化还原反应中电子转移守恒计算.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
4.下列说法中不 正确的是( )
| A. | 1 mol CH≡CH可以与Br2发生加成反应,消耗2 mol Br2 | |
| B. | 苯的邻位二元取代物只有一种可以说明苯分子不具有碳碳单键和碳碳双键的交替结构 | |
| C. | 2甲基戊烷的沸点高于己烷 | |
| D. | 用水可区分苯和溴苯 |
2.决定化学反应速率的主要因素是( )
| A. | 温度 | B. | 反应物的性质 | C. | 浓度 | D. | 催化剂 |
6.下列关于物质检验或鉴别的说法错误的是( )
| A. | 用CCl4鉴别溴水和碘水 | |
| B. | 用AgNO3溶液鉴别溴化钾溶液和氯化钠溶液 | |
| C. | 向某盐溶液中加入氢氧化钠溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,溶液中一定有NH4+ | |
| D. | 向某盐溶液中,加入盐酸,产生使澄清石灰水变浑浊的气体,溶液中含有大量CO32-离子 |
13.下面是一些常见分子的比例模型.其中1个分子中含有共用电子对最多的是( )
| A. |  氢气 | B. |  氨气 | C. |  水 | D. |  二氧化碳 |
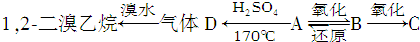 若有A、B、C三种烃的衍生物,相互转化关系如图:C跟石灰石反应产生使石灰水变浑浊的气体.
若有A、B、C三种烃的衍生物,相互转化关系如图:C跟石灰石反应产生使石灰水变浑浊的气体.