题目内容
CO2通入下列各溶液中,不可能产生沉淀的是( )
| A、CaCl2溶液 |
| B、石灰水 |
| C、Ca(ClO)2溶液 |
| D、Na2SiO3溶液 |
考点:钠的重要化合物,氯、溴、碘及其化合物的综合应用
专题:
分析:二氧化碳通入下列溶液中,不可能产生沉淀,说明二氧化碳不和该物质反应或生成可溶性物质,据此分析解答.
解答:
解:A.碳酸的酸性小于盐酸,所以二氧化碳和氯化钙溶液不反应,则不可能产生沉淀,故A正确;
B.少量二氧化碳和石灰水反应方程式为CO2+Ca(OH)2=CaCO3↓+H2O,过量二氧化碳和氢氧化钙反应为Ca(OH)2+2CO2=Ca(HCO3)2,所以二氧化碳通入石灰水中可能不产生沉淀,也可能产生沉淀,故B错误;
C.Ca(C1O)2溶液中通入少量的二氧化碳生成次氯酸和碳酸钙沉淀,通入过量的二氧化碳生成次氯酸和碳酸氢钙,所以二氧化碳通入Ca(C1O)2溶液中可能不产生沉淀,也可能产生沉淀,故C错误;
D.硅酸钠溶液和二氧化碳反应为Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3,所以有沉淀生成,故D错误;
故选A.
B.少量二氧化碳和石灰水反应方程式为CO2+Ca(OH)2=CaCO3↓+H2O,过量二氧化碳和氢氧化钙反应为Ca(OH)2+2CO2=Ca(HCO3)2,所以二氧化碳通入石灰水中可能不产生沉淀,也可能产生沉淀,故B错误;
C.Ca(C1O)2溶液中通入少量的二氧化碳生成次氯酸和碳酸钙沉淀,通入过量的二氧化碳生成次氯酸和碳酸氢钙,所以二氧化碳通入Ca(C1O)2溶液中可能不产生沉淀,也可能产生沉淀,故C错误;
D.硅酸钠溶液和二氧化碳反应为Na2SiO3+CO2+H2O=H2SiO3↓+Na2CO3,所以有沉淀生成,故D错误;
故选A.
点评:本题考查了物质间的反应,明确物质的性质是解本题关键,根据物质的溶解性、酸的强弱等知识点即可解答,题目难度不大.

练习册系列答案
相关题目
胶体区别于其它分散系最本质的特征是( )
| A、外观澄清、透明 |
| B、分散质粒子能透过半透膜 |
| C、丁达尔现象 |
| D、胶体粒子直径在1~100nm之间 |
下列有关碳酸钠、碳酸氢钠的说法中,正确的是( )
| A、除去碳酸氢钠固体中混有的少量碳酸钠可以采用加热的方法 |
| B、相同条件下,碳酸钠的溶解度小于碳酸氢钠的溶解度 |
| C、碳酸钠与盐酸反应放出二氧化碳的剧烈程度强于碳酸氢钠 |
| D、同浓度的碳酸钠溶液和碳酸氢钠溶液,碳酸氢钠溶液的碱性弱 |
下列溶液中离子一定能够大量共存的是( )
| A、加入Al能放出H2的溶液中:Cl-、SO42-、NO3-、Mg2+ |
| B、能使淀粉碘化钾试纸显蓝色的溶液中:K+、SO42-、S2-、SO32- |
| C、c(H+):c(OH-)=1:1012的水溶液中:CO32-、Na+、NO3-、AlO2- |
| D、无色溶液中:K+、Na+、MnO4-、SO42- |
X是铁与硫在隔绝空气的条件下反应后所得固体,倾斜A使稀硫酸(足量)与固体X充分反应,等反应停止后,B装置质量增加,C装置中溶液无变化.反应后进入量气管气体的体积VmL(已折算成标准状况),下列说法正确的是( )
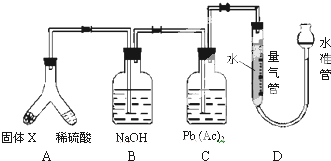

| A、固体X中一定有的物质是FeS、Fe 和S |
| B、B装置中的溶质一定是Na2S |
| C、C装置的作用是检验H2S是否完全被吸收 |
| D、X中其中一种物质的质量为V/400g |
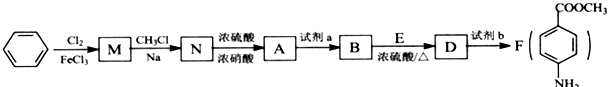
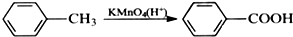
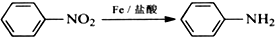
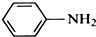 苯胺,弱碱性,-NH2易被氧化成-NO2
苯胺,弱碱性,-NH2易被氧化成-NO2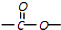 结构;
结构;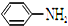 最多能够和
最多能够和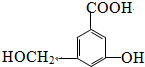
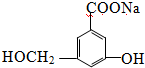
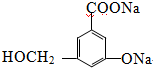
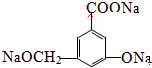 .
.