题目内容
8.铅蓄电池放电时的反应:PbO2+Pb+2H2SO4═2PbSO4+2H2O,下列有关放电时的说法正确的是( )| A. | PbO2作正极,电极发生氧化反应 | |
| B. | 当转移的电子数为3.01×1023时,参与反应的Pb的质量为103.5 g | |
| C. | 负极的电极反应式是:Pb+SO42--2e-═PbSO4 | |
| D. | 溶液中H+移向负极 |
分析 该原电池放电时,正极反应式为PbO2+4H++SO42--2e-═2H2O+PbSO4,负极反应式为Pb+SO42--2e-═PbSO4,
A.PbO2作正极,得电子的物质发生还原反应;
B.根据Pb+SO42--2e-═PbSO4计算消耗Pb的质量;
C.负极上Pb失电子发生氧化反应;
D.放电时,电解质溶液中阳离子向正极移动,阴离子向负极移动.
解答 解:该原电池放电时,正极反应式为PbO2+4H++SO42--2e-═2H2O+PbSO4,负极反应式为Pb+SO42--2e-═PbSO4,
A.PbO2作正极,正极反应式为PbO2+4H++SO42--2e-═2H2O+PbSO4,二氧化铅得电子发生还原反应,故A错误;
B.当转移的电子数为3.01×1023时,转移电子物质的量是0.5mol,根据Pb+SO42--2e-═PbSO4得消耗n(Pb)=$\frac{0.5mol}{2}×1$=0.25mol,消耗Pb质量=0.25mol×207g/mol=51.75g,故B错误;
C.负极上Pb失电子发生氧化反应,电极反应式为Pb+SO42--2e-═PbSO4,故C正确;
D.放电时,电解质溶液中阳离子向正极移动,阴离子向负极移动,所以溶液中H+移向正极,故D错误;
故选C.
点评 本题考查原电池原理,为高频考点,明确正负极与元素化合价变化关系是解本题关键,难点是电极反应式的书写及有关计算,注意电解质溶液中阴阳离子移动方向,为易错点.

练习册系列答案
相关题目
19.下列关于物质的相互关系正确的是( )
| A. | ${\;}_{\;}^{12}C$ 与${\;}_{\;}^{14}C$互为同素异形体 | |
| B. | 金刚石与石墨互为同位素 | |
| C. | 二甲醚与乙醇互为同分异构体 | |
| D. | 乙烷与乙烯互为同系物 |
16.甲、乙、丙、丁4种易溶于水的物质,分别由NH4+、Ba2+、Mg2+、H+、HCO3-、SO42-、OH-、Cl-中的不同阳离子和阴离子各一种组成.已知:①将足量的甲溶液分别与其他3种物质的溶液混合,均有白色沉淀生成;②0.1mol?L-1乙溶液中c(H+)>0.1mol?L-1;③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成.下列结论正确的是( )
| A. | 甲溶液含有Ba2+ | B. | 乙溶液不含SO42- | C. | 丙溶液含有HCO3- | D. | 丁溶液含有Mg2+ |
3.电渗析法是指在外加电场作用下,利用阴离子交换膜和阳离子交换膜的选择透过性,使部分离子透过离子交换膜而迁移到另一部分水中,从而使一部分水淡化而另一部分水浓缩的过程.下图是利用电渗析法从海水中获得淡水的原理图,已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为石墨电极.下列有关描述错误的是( )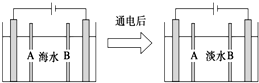

| A. | 阳离子交换膜是A,不是B | |
| B. | 通电后阳极区的电极反应式:2Cl--2e-═Cl2↑ | |
| C. | 工业上阴极使用铁丝网代替石墨碳棒,增大反应接触面 | |
| D. | 阴极区的现象是电极上产生无色气体,溶液中出现少量白色沉淀 |
13.下列各组微粒在指定的环境中一定大量存在的是( )
| A. | 与铝反应产生H2的溶液中:Na+、K+、S2-、CO32- | |
| B. | 加入酚酞显红色的溶液中:K+、Na+、Cl-、CH3COO- | |
| C. | pH=2的溶液中:NH4+、Na+、Fe2+、NO3-、Cl- | |
| D. | 由水电离出的c(H+)=1×10-12mol•L-1的溶液中:K+、Na+、Cl-、Al3+ |
17.已知溴(Br2)的性质与Cl2相似,将溴水加人含有下列离子的溶液中,离子浓度变化最小的是( )
| A. | Fe2+ | B. | HCO3- | C. | Fe3+ | D. | OH- |
18.在无色透明的酸性溶液中,能大量共存的离子组是( )
| A. | Na+、Ca2+、Cl-、SO42- | B. | Fe2+、Na+、ClO、NO3- | ||
| C. | MnO4-、K+、SO42-、Na+ | D. | Mg2+、NH4+、Cl-、SO42- |
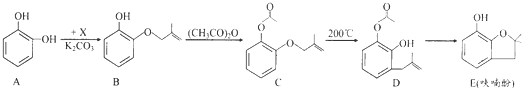
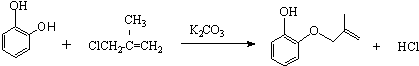 .
.