题目内容
下列变化不属于水解反应的是( )
| A、NH4++H2O?NH3?H2O+H+ |
| B、HS-+H2O?H3O++S2- |
| C、HS-+H2O?H2S+OHˉ |
| D、NH4++2H2O?NH3?H2O+H3O+ |
考点:盐类水解的原理
专题:盐类的水解专题
分析:根据水解反应的定义:盐电离出的弱酸或弱碱离子与水电离产生的氢离子或氢氧根离子结合生成弱电解质的反应,以此来解答.
解答:
解:A.NH4++H2O?NH3?H2O+H+为NH4+的水解,生成NH3?H2O,水解呈酸性,故A不选;
B.为HS-的电离方程式,故B选;
C.HS-+H2O?H2S+OHˉ为HSˉ的水解方程式,水解生成H2S,溶液呈碱性,故C不选;
D.NH4++2H2O?NH3?H2O+H3O+为NH4+的水解,生成NH3?H2O,水解呈酸性,故D不选.
故选B.
B.为HS-的电离方程式,故B选;
C.HS-+H2O?H2S+OHˉ为HSˉ的水解方程式,水解生成H2S,溶液呈碱性,故C不选;
D.NH4++2H2O?NH3?H2O+H3O+为NH4+的水解,生成NH3?H2O,水解呈酸性,故D不选.
故选B.
点评:本题考查盐类水解原理、水解离子方程式的分析判断,注意电离方程式的理解应用,特别是H2S、H2O的电离方程式的判断,题目难度中等.

练习册系列答案
相关题目
科学家已发现一种新型氢分子H3,在相同条件下,等质量的H3和H2相同的是( )
| A、密度 | B、分子数 |
| C、电子数 | D、体积 |
据报载我国最近合成了多种元素的新的原子,测定了铪(Hf)元素的相对原子质量的新值.铪元素的核电荷数为72,相对原子质量为185,铪原子的中子数为( )
| A、72 | B、113 |
| C、185 | D、257 |
在高温下,反应2HBr(g)?Br2(g)+H2(g)△H>0达到平衡时要使混合气体颜色加深,不能采用的方法是( )
| A、增大HBr浓度 |
| B、缩小容器体积 |
| C、升高温度 |
| D、增大H2的浓度 |
下列说法中正确的是( )
| A、溶液与胶体:本质不同的原因是能否发生丁达尔效应 |
| B、用托盘天平称得2.50 g胆矾,受热充分失水后,固体质量减轻0.90g |
| C、从1L 1mol?L-1的NaCl溶液中取出10 mL,其浓度仍是1mol?L-1 |
| D、10g 98%硫酸(密度为1.84 g/cm3)与10mL 18.4mol?L-1硫酸的浓度是不同的 |
设NA为阿伏伽德罗常数的数值,则下列说法中不正确的是( )
①2.24L氖气含有NA个电子,②18g D2O中所含的中子数为10NA,③标准状况下,11.2L SO3含有的分子数为0.5NA,④过氧化钠与水反应,若电子转移2NA,则产生的氧气为32g,⑤在1L 0.1mol/L的碳酸钠溶液中,氧原子总数为0.3NA.
①2.24L氖气含有NA个电子,②18g D2O中所含的中子数为10NA,③标准状况下,11.2L SO3含有的分子数为0.5NA,④过氧化钠与水反应,若电子转移2NA,则产生的氧气为32g,⑤在1L 0.1mol/L的碳酸钠溶液中,氧原子总数为0.3NA.
| A、①②③⑤ | B、①④⑤ |
| C、①②③ | D、②③⑤ |
已知NaCl、CsCl晶体结构中离子配位数分别为6和8,其中属于从NaCl晶体中分割出来的结构示意图是( )
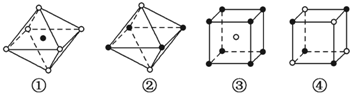

| A、①和③ | B、①和④ |
| C、只有③ | D、只有④ |
关于热化学方程式:2H2(g)+02(g)═2H20(1),△H=-571.6kJ?mol-1,下列有关叙述不正确的
( )
( )
| A、2mol H2完全燃烧生成液态水时放出571.6kJ的热量 | ||
| B、1mol H2完全燃烧生成液态水时放出285.8kJ的热量 | ||
| C、2个氢分子完全燃烧生成液态水时放出571.6 kJ的热量 | ||
D、上述热化学方程式可表示为H2(g)+
|