题目内容
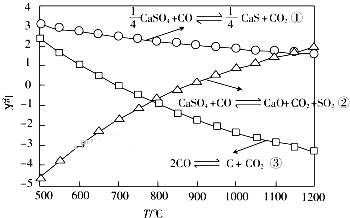 一氧化碳在高温下可还原硫酸钙,相关反应的平衡常数的对数与反应温度的关系如图所示.
一氧化碳在高温下可还原硫酸钙,相关反应的平衡常数的对数与反应温度的关系如图所示.(l)已知:CaSO4(s)+4CO(g)?CaS(s)+4CO2(g)△H1=-175.6kJ?mol-1 lgK1
CaSO4(s)+CO(g)?CaO(s)+SO2(g)+CO2(g)△H2=+218.4kJ?mol-1 lgK2
CaS(s)+3CaSO4(s)?4CaO(s)+4SO2(g)△H3 lgK3
则△H3=
(2)反应2CO(g)?C(s)+CO2(g)的△H
(3)500℃时,反应
| 1 |
| 4 |
| 1 |
| 4 |
(4)恒温恒容条件下,下列说法中,能判断反应2CO(g)?C(s)+CO2(g) 一定达到平衡状态的是
A.CO和CO2的反应速率之比为2:1 B.单位时间内,消耗2mol CO的同时生成1molCO2
C.CO2的体积分数保持不变 D.混合气体的密度保持不变.
考点:化学平衡的计算,热化学方程式,化学平衡的影响因素
专题:
分析:(1)根据盖斯定律计算;
(2)反应2CO(g)?C(s)+CO2(g)温度升高,平衡常数减小,即平衡逆向移动;平衡常数不包含固体和纯液体;
(3)500℃时,反应
CaSO4(s)+CO(g)?
CaS(s)+CO2(g)lgK=3,即平衡常数K=1000;
(4)平衡状态时正逆反应速率相等,各组分含量不变.
(2)反应2CO(g)?C(s)+CO2(g)温度升高,平衡常数减小,即平衡逆向移动;平衡常数不包含固体和纯液体;
(3)500℃时,反应
| 1 |
| 4 |
| 1 |
| 4 |
(4)平衡状态时正逆反应速率相等,各组分含量不变.
解答:
解:已知:①CaSO4(s)+4CO(g)?CaS(s)+4CO2(g)△H1=-175.6kJ?mol-1 lgK1
②CaSO4(s)+CO(g)?CaO(s)+SO2(g)+CO2(g)△H2=+218.4kJ?mol-1 lgK2
由②×4-①可得CaS(s)+3CaSO4(s)?4CaO(s)+4SO2(g)△H3=lgK3,则△H3=4lgK2-lgK1=4×(+218.4kJ?mol-1)-(-175.6kJ?mol-1)=+1049.2kJ?mol-1,
故答案为:+1049.2kJ?mol-1;4lgK2-lgK1;
(2)反应2CO(g)?C(s)+CO2(g)温度升高,平衡常数减小,即平衡逆向移动,正反应放热,△H<0,平衡常数K=
,反应2CO(g)?C(s)+CO2(g)△H<0,升温,平衡逆向移动,故答案为:<;
;升温;
(3)500℃时,反应
CaSO4(s)+CO(g)?
CaS(s)+CO2(g)lgK=3,平衡常数K=
=1000,故CO2与CO的物质的量之比为1000,故答案为:1000;
(4)恒温恒容条件下,反应2CO(g)?C(s)+CO2(g),
A.任何状态时CO和CO2的反应速率之比为2:1,所以不能说明反应达到平衡状态,故A错误;
B.任何状态时,单位时间内,消耗CO与生成CO2的物质的量之比为计量数之比,即2:1,所以消耗2mol CO的同时生成1molCO2,不能说明反应达到平衡状态,故B错误;
C.CO2的体积分数保持不变,正逆反应速率相等,反应达到平衡状态,故C正确;
D.气体质量减小,体积不变,混合气体的密度减小,若混合气体密度保持不变说明反应达到平衡状态,故D正确.
故答案为:CD.
②CaSO4(s)+CO(g)?CaO(s)+SO2(g)+CO2(g)△H2=+218.4kJ?mol-1 lgK2
由②×4-①可得CaS(s)+3CaSO4(s)?4CaO(s)+4SO2(g)△H3=lgK3,则△H3=4lgK2-lgK1=4×(+218.4kJ?mol-1)-(-175.6kJ?mol-1)=+1049.2kJ?mol-1,
故答案为:+1049.2kJ?mol-1;4lgK2-lgK1;
(2)反应2CO(g)?C(s)+CO2(g)温度升高,平衡常数减小,即平衡逆向移动,正反应放热,△H<0,平衡常数K=
| c(CO2) |
| c(CO) |
| c(CO2) |
| c(CO) |
(3)500℃时,反应
| 1 |
| 4 |
| 1 |
| 4 |
| c(CO2) |
| c(CO) |
(4)恒温恒容条件下,反应2CO(g)?C(s)+CO2(g),
A.任何状态时CO和CO2的反应速率之比为2:1,所以不能说明反应达到平衡状态,故A错误;
B.任何状态时,单位时间内,消耗CO与生成CO2的物质的量之比为计量数之比,即2:1,所以消耗2mol CO的同时生成1molCO2,不能说明反应达到平衡状态,故B错误;
C.CO2的体积分数保持不变,正逆反应速率相等,反应达到平衡状态,故C正确;
D.气体质量减小,体积不变,混合气体的密度减小,若混合气体密度保持不变说明反应达到平衡状态,故D正确.
故答案为:CD.
点评:本题考查了盖斯定律的应用、平衡常数的计算以及化学平衡状态的判断,难度中等,注意平衡常数公式中不包含固体和纯液体.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
NaHS、MgSO4、NaHSO4三种物质组成的混合物中,已知氧元素的质量分数为a%,则其中硫元素的质量分数为( )
| A、a% | ||
| B、1-1.75 a% | ||
C、
| ||
D、
|
关于酚羟基和醇羟基的分析中,错误的是( )
| A、原子组成一样 |
| B、O-H键的化学键类型一样 |
| C、羟基中氢原子活性性不同 |
| D、酚羟基能发生电离,醇羟基也能发生电离 |
物质对应的用途(括号内是用途)错误的是( )
| A、单质硅(光导纤维) |
| B、钠钾合金(原子反应堆导热剂) |
| C、过氧化钠(潜水艇中供氧剂) |
| D、硫酸钡(医疗钡餐) |
下列说法不正确的是( )
| A、分子式为C3H8与C6H14的两种有机物一定互为同系物 |
| B、对有机物分子红外光谱图的研究有助于确定有机物分子中的基团 |
| C、分子式C4H10表示的物质必是纯净物 |
D、有机物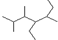 的名称:2,3,5-三甲基-4-乙基庚烷 的名称:2,3,5-三甲基-4-乙基庚烷 |
向含有Cu(NO3)2,Zn(NO3)2,Fe(NO3)3,AgNO3各0.1mol的混合溶液中加入0.1mol铁粉,充分搅拌反应后,下列结论错误的是( )
| A、溶液中析出0.05mol Cu |
| B、溶液中析出0.1mol Ag |
| C、溶液中Cu2+与Fe2+的浓度之比为1:2 |
| D、往反应后的溶液中再加入0.1mol 铁粉,铁粉恰好完全溶解 |
区分氢氧化铁胶体与含酚酞的稀氢氧化钠混合溶液最简便有效的方法是( )
| A、滴加盐酸 | B、丁达尔效应 |
| C、过滤 | D、蒸馏 |
 (1)将下列离子Na+、K+、Cu2+、H+、NO3-、Cl-、CO32-、OH-,按可能大量共存于同一溶液的情况,则分成A、B两组,而且每组中均含两种阳离子和两种阴离子,则A组
(1)将下列离子Na+、K+、Cu2+、H+、NO3-、Cl-、CO32-、OH-,按可能大量共存于同一溶液的情况,则分成A、B两组,而且每组中均含两种阳离子和两种阴离子,则A组