题目内容
3.短周期元素X、Y、Z、W、R的化合价与原子序数的关系如下图所示.下列说法正确的是( )
| A. | 离子半径:W3+>Z+>Y2- | |
| B. | X、Y都存在同素异形现象 | |
| C. | Z和Y形成的化合物中只存在离子键 | |
| D. | 常温下单质W能溶于R的最高价氧化物对应水化物的浓溶液 |
分析 X、Y、Z、W、R为短周期元素,有两种元素既有+4价,又有-4价,故前一种元素为碳,后一种元素为硅,故X为C元素;Y的化合价为-2价,没有正化合价,故Y为O元素,Z的化合价为+1价,处于ⅠA族,原子序数大于O元素,故Z为Na元素;W为+3价,为Al元素,R的化合价为+6、-2价,故R为S元素,结合元素化合物的性质及元素周期律解答.
解答 解:X、Y、Z、W、R为短周期元素,有两种元素既有+4价,又有-4价,故前一种元素为碳,后一种元素为硅,故X为C元素;Y的化合价为-2价,没有正化合价,故Y为O元素,Z的化合价为+1价,处于ⅠA族,原子序数大于O元素,故Z为Na元素;W为+3价,为Al元素,R的化合价为+6、-2价,故R为S元素.
A.电子排布相同的微粒,原子序数越大,离子半径越小,则离子半径:O2->Na+>Al3+,故A错误;
B.X为C元素,Y为O元素,C、O元素均存在同分异构体,故B正确;
C.Na和O形成的化合物Na2O2中存在离子键和共价键,故C错误;
D.常温下Al在浓硫酸中会钝化,故D错误;
故选B.
点评 本题考查结构性质与位置关系、元素周期律等,难度不大,根据推断元素是解题的关键,根据化合价结合原子序数进行推断,侧重于考查学生的分析能力和对基础知识的应用能力.

练习册系列答案
相关题目
14.下列各组离子在指定溶液中一定能大量共存的是( )
| A. | 使甲基橙变红色的溶液:Al3+、Cu2+、I-、S2O32- | |
| B. | 常温下加水稀释时c(H+)/c(OH-)明显增大的溶液:CH3COO-、Ba2+、NO3-、Br- | |
| C. | 0.1mol/LFe(NO3)2溶液:S2-、Na+、SO42-、Cl- | |
| D. | 0.1mol/LNaAlO2溶液:NH4+、K+、HCO3-、SO32- |
11.常温下,下列溶液中的微粒浓度关系正确的是( )
| A. | pH=5的CH3COOH溶液和pH=5的NH4Cl溶液中,c(H+)不相等 | |
| B. | pH=8.3的NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | 0.1 mol AgCl和0.1 mol AgI混合后加入1 L水中,所得溶液中:c(Cl-)=c(I-) | |
| D. | 0.2 mol/L CH3COOH溶液与0.1 mol/L NaOH溶液等体积混合后所得溶液中:2c(H+)-2c(OH-)=c(CH3COO-)-c(CH3COOH) |
12.下列物质中含碳质量分数最高的是( )
| A. | 苯 | B. | 辛烯 | C. | 辛烷 | D. | 十六烷 |
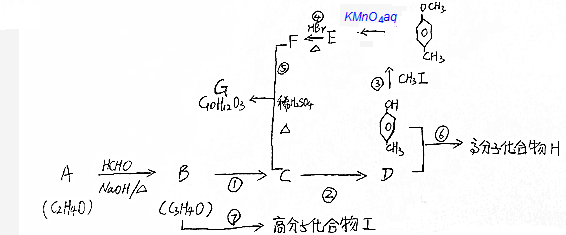

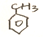 $\stackrel{KMnO_{4}aq}{→}$
$\stackrel{KMnO_{4}aq}{→}$
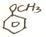 $→_{△}^{HBr}$
$→_{△}^{HBr}$ 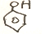
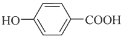 +CH3CH2CH2OH$→_{△}^{浓硫酸}$
+CH3CH2CH2OH$→_{△}^{浓硫酸}$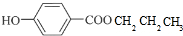 +H2O
+H2O
 .W、X、Y的离子半径由大到小的顺序为S2->O2->Al3+(用离子符号回答)
.W、X、Y的离子半径由大到小的顺序为S2->O2->Al3+(用离子符号回答)