题目内容
17克NH3共有 mol原子,0.1molH2S共有 个氢原子;同质量的NH3和H2S中分子个数比为 .在标准状况下,35.5g氯气的体积是 L,将其与氢气完全化合,需氢气的物质的量是 mol,将生成的气体配制成1L溶液,溶质的物质的量浓度是 mol?L-1,将此溶液取出20mL加蒸馏水制成200mL溶液,此冲稀后溶液中溶质的物质的量浓度是 mol?L-1.
【答案】分析:根据n=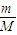 =
=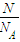 =
=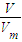 结合分子的构成,以及c=
结合分子的构成,以及c=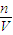 计算有关物理量.
计算有关物理量.
解答:解:n(NH3)=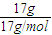 =1mol,所含原子的物质的量为4mol;
=1mol,所含原子的物质的量为4mol;
0.1molH2S共有0.2NA个氢原子;
由n=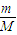 =
=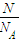 可知:N(NH3):N(H2S)=
可知:N(NH3):N(H2S)=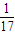 :
: =2:1;
=2:1;
n(Cl2)=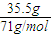 =0.5mol,V(Cl2)=0.5mol×22.4L/mol=11.2L;
=0.5mol,V(Cl2)=0.5mol×22.4L/mol=11.2L;
由反应Cl2+H2=2HCl可知:需氢气的物质的量是0.5mol;
c(HCl)=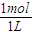 =1mol/L;
=1mol/L;
将此溶液取出20mL加蒸馏水制成200mL溶液,此冲稀后溶液中溶质的物质的量浓度是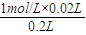 =0.1mol/L.
=0.1mol/L.
故答案为:4;0.2NA;2:1;11.2L;0.5;1;0.1.
点评:本题考查物质的量的相关计算,题目难度不大,注意有关计算公式的运用.
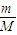 =
=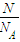 =
=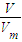 结合分子的构成,以及c=
结合分子的构成,以及c=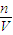 计算有关物理量.
计算有关物理量.解答:解:n(NH3)=
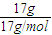 =1mol,所含原子的物质的量为4mol;
=1mol,所含原子的物质的量为4mol;0.1molH2S共有0.2NA个氢原子;
由n=
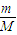 =
=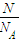 可知:N(NH3):N(H2S)=
可知:N(NH3):N(H2S)=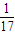 :
: =2:1;
=2:1;n(Cl2)=
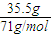 =0.5mol,V(Cl2)=0.5mol×22.4L/mol=11.2L;
=0.5mol,V(Cl2)=0.5mol×22.4L/mol=11.2L;由反应Cl2+H2=2HCl可知:需氢气的物质的量是0.5mol;
c(HCl)=
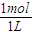 =1mol/L;
=1mol/L;将此溶液取出20mL加蒸馏水制成200mL溶液,此冲稀后溶液中溶质的物质的量浓度是
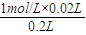 =0.1mol/L.
=0.1mol/L.故答案为:4;0.2NA;2:1;11.2L;0.5;1;0.1.
点评:本题考查物质的量的相关计算,题目难度不大,注意有关计算公式的运用.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目