题目内容
 某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法不正确的是( )
某溶液中可能含有H+、NH4+、Mg2+、Al3+、Fe3+、CO32-、SO42-、NO3-中的几种.①若加入锌粒,产生无色无味的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入NaOH的物质的量之间的关系如图所示.则下列说法不正确的是( )| A、溶液中的阳离子有H+、Mg2+、NH4+、Al3+ |
| B、溶液中n (Al3+)=0.2mol |
| C、溶液中一定不含CO32-,可能含有SO42-和NO3- |
| D、n(H+):n(Al3+):n(Mg2+)=2:2:1 |
考点:常见阳离子的检验,常见阴离子的检验
专题:物质检验鉴别题
分析:若加入锌粒,产生无色无味无毒的气体,说明气体是氢气,因此溶液显酸性,则CO32-和NO3-不能大量共存;加入NaOH溶液,产生白色沉淀,说明不存在铁离子;根据产生的沉淀量与加入NaOH的物质的量之间的关系图可知,溶液中一定含有Mg2+、Al3+;又因为当沉淀达到最大值时,继续进入氢氧化钠,沉淀不变,这说明溶液中还存在NH4+,由于溶液中还必须存在阴离子,所以一定还有SO42-.结合图象中各阶段消耗的氢氧化钠,计算溶液中n(H+)、n(Mg2+)、n(Al3+)、n(NH4+),据此解答.
解答:
解:若加入锌粒,产生无色无味无毒的气体,说明气体是氢气,因此溶液显酸性,则CO32-和NO3-不能大量共存;
加入NaOH溶液,产生白色沉淀,说明不存在Fe3+;根据产生的沉淀量与加入NaOH的物质的量之间的关系图可知,溶液中一定含有Mg2+、Al3+;又因为当沉淀达到最大值时,继续进入氢氧化钠,沉淀不变,这说明溶液中还存在NH4+,由于溶液中还必须存在阴离子,所以一定还有SO42-;
由图象可知,第一阶段为氢离子与氢氧化钠反应,消耗氢氧化钠为0.1mol,则n(H+)=0.1mol;
第三阶段为铵根离子与氢氧化钠反应,消耗氢氧化钠为0.7mol-0.5mol=0.2mol,则n(NH4+)=0.2mol;
最后阶段为氢氧化钠溶解氢氧化铝,消耗氢氧化钠0.8mol-0.7mol=0.1mol,则n[Al(OH)3]=0.1mol,根据铝元素守恒可知n(Al3+)=0.1mol;
第二阶段为氢氧化钠沉淀镁离子、铝离子,共消耗氢氧化钠为0.5mol-0.1mol=0.4mol,则n(Mg2+)=(0.4mol-0.1mol×3)÷2=0.05mol,
A.由上述分析可知,溶液中的阳离子只有H+、Mg2+、Al3+、NH4+,故A正确,不选;
B.由上述分析可知,溶液中n(Al3+)=0.1mol;故B错误,故选;
C.由上述分析可知,溶液中一定不含CO32-、NO3-,一定含有SO42-,故C错误,故选;
D.由上述分析可知,溶液中n(H+):n(Al3+):n(Mg2+)=0.1mol:0.1mol:0.05mol=2:2:1,故D正确,不选,
故选BC.
加入NaOH溶液,产生白色沉淀,说明不存在Fe3+;根据产生的沉淀量与加入NaOH的物质的量之间的关系图可知,溶液中一定含有Mg2+、Al3+;又因为当沉淀达到最大值时,继续进入氢氧化钠,沉淀不变,这说明溶液中还存在NH4+,由于溶液中还必须存在阴离子,所以一定还有SO42-;
由图象可知,第一阶段为氢离子与氢氧化钠反应,消耗氢氧化钠为0.1mol,则n(H+)=0.1mol;
第三阶段为铵根离子与氢氧化钠反应,消耗氢氧化钠为0.7mol-0.5mol=0.2mol,则n(NH4+)=0.2mol;
最后阶段为氢氧化钠溶解氢氧化铝,消耗氢氧化钠0.8mol-0.7mol=0.1mol,则n[Al(OH)3]=0.1mol,根据铝元素守恒可知n(Al3+)=0.1mol;
第二阶段为氢氧化钠沉淀镁离子、铝离子,共消耗氢氧化钠为0.5mol-0.1mol=0.4mol,则n(Mg2+)=(0.4mol-0.1mol×3)÷2=0.05mol,
A.由上述分析可知,溶液中的阳离子只有H+、Mg2+、Al3+、NH4+,故A正确,不选;
B.由上述分析可知,溶液中n(Al3+)=0.1mol;故B错误,故选;
C.由上述分析可知,溶液中一定不含CO32-、NO3-,一定含有SO42-,故C错误,故选;
D.由上述分析可知,溶液中n(H+):n(Al3+):n(Mg2+)=0.1mol:0.1mol:0.05mol=2:2:1,故D正确,不选,
故选BC.
点评:本题考查离子共存、反应图象识别以及离子反应有关计算等,是高考中的常见题型,对学生的综合能力提出了更高的要求,有利于培养学生的逻辑思维能力和发散思维能力,难度较大.

练习册系列答案
相关题目
已知反应:①SeO2+4KI═Se+2I2+4KI+2H2O;②Se+2H2SO4(浓)═2SO2↑+SeO2+2H2O.下列叙述正确的是( )
| A、反应①中Se是氧化产物,I2是还原产物 |
| B、反应②中浓H2SO4是氧化剂,SeO2是还原产物 |
| C、反应①中每有1.0mol I2生成,转移电子数目为4NA |
| D、SeO2、H2SO4(浓)、I2的氧化性由强到弱的顺序是H2SO4(浓)>SeO2>I2 |
某温度下,密闭容器中X、Y、Z、W四种气体的初始浓度和平衡浓度如下表,下列说法错误的是( )
| 物质 | X | Y | Z | W |
| 初始浓度/mol?L-1 | 0.5 | 0.6 | 0 | 0 |
| 平衡浓度/mol?L-1 | 0.1 | 0.1 | 0.4 | 0.6 |
| A、反应达到平衡时,X的转化率为80% | ||
B、该反应的平衡常数表达式为K=
| ||
| C、增大压强其平衡常数不变,但使平衡向生成Z的方向移动 | ||
| D、改变温度可以改变此反应的平衡常数 |
下列反应的离子方程式正确的是( )
| A、用FeCl3溶液腐蚀印刷电路板:2Fe3++Cu═2Fe2++Cu2+ |
| B、氢氧化钡溶液跟硫酸反应:OH-+H+═H2O |
| C、碳酸钙与盐酸反应:2H++CO32-=H2O+CO2↑ |
| D、氧化铜与稀硫酸混合:CuO+H+═Cu2++H2O |
下列图示与对应的叙述相符的是( )
A、 表示的反应速率随温度变化的关系可知该反应的△H>0 |
B、 代表等物质的量的气体A和B,在一定温度下发生反应A(g)+B(g)?2C(g),达到平衡后,只改变反应的一个条件,其在20~40 min之间的平衡常数不相等 |
C、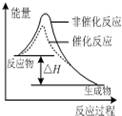 表示该反应为放热反应,且催化剂不能改变反应的焓变 |
D、 表示向Na2CO3溶液中逐滴滴加稀盐酸,生成CO2与所加盐酸物质的量的关系 |


 某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如表:
某化学小组以苯甲酸为原料,制取苯甲酸甲酯,已知有关物质的沸点如表:
