题目内容
(1)MnO2可做超级电容器材料,用惰性电极电解MnSO4溶液可制得MnO2,其阳极的电极反应式是 .
(2)MnO2是碱性锌锰电池的正极材料,碱性锌锰电池放电时,正极的电极反应式是 .
(2)MnO2是碱性锌锰电池的正极材料,碱性锌锰电池放电时,正极的电极反应式是
考点:电极反应和电池反应方程式
专题:电化学专题
分析:(1)根据电解原理用惰性电极电解MnSO4溶液制得MnO2的阳极为Mn2+失电子发生氧化反应生成MnO2;
(2)根据原电池工作原理正极MnO2得电子发生还原反应.
(2)根据原电池工作原理正极MnO2得电子发生还原反应.
解答:
解:(1)电解池中阳极失去电子发生氧化反应,则用惰性电极电解MnSO4溶液可制得MnO2,因此阳极是锰离子放电,其阳极电极反应式是Mn2++2H2O-2e-=MnO2+4H+,故答案为:Mn2++2H2O-2e-=MnO2+4H+;
(2)原电池中负极失去电子,正极得到电子,因此碱性锌锰电池放电时,正极是二氧化锰得到电子,则电极反应式为:MnO2+H2O+e-=MnO(OH)+OH-,
故答案为:MnO2+H2O+e-═MnOOH+OH-.
(2)原电池中负极失去电子,正极得到电子,因此碱性锌锰电池放电时,正极是二氧化锰得到电子,则电极反应式为:MnO2+H2O+e-=MnO(OH)+OH-,
故答案为:MnO2+H2O+e-═MnOOH+OH-.
点评:本题考查了电极反应式的书写,注意抓住原理分析解答,难度不大.

练习册系列答案
 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案
相关题目
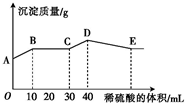 将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解后,向混合溶液中滴加1mol?L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断正确的是( )
将由NaOH、BaCl2、Al2(SO4)3三种固体组成的混合物溶于足量的水中,充分溶解后,向混合溶液中滴加1mol?L-1的稀硫酸,加入稀硫酸的体积与生成沉淀的质量关系如图所示.下列有关判断正确的是( )| A、AB段发生反应的离子方程式为Ba2++SO42-═BaSO4↓ |
| B、BC段发生反应的离子方程式为H++OH-=H2O |
| C、D点表示的沉淀的化学式为Al(OH)3 |
| D、E点时溶液中含有AlO2- |
关于NaHCO3溶液的表述正确的是( )
| A、c (Na+)=c (HCO3-)+c (CO32-)+c (H2CO3) |
| B、c (Na+)+c (H+)=c (HCO3-)+c (CO32-)+c (OH-) |
| C、HCO3- 的电离程度大于HCO3-的水解程度 |
| D、其电离方程式为:NaHCO3?Na++H++CO32- |
在电解水的实验中需要加少量电解质来增强水的导电性.下列属于电解质,且加入水中能增强导电性的是( )
| A、铜 |
| B、NaOH |
| C、H2SO4溶液 |
| D、BaSO4 |
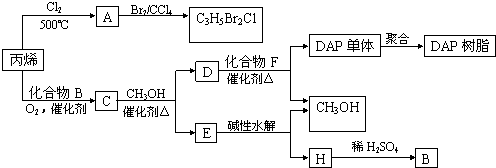

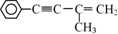 的反应条件是
的反应条件是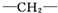 ,一个
,一个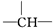 ,则X的结构简式为
,则X的结构简式为