题目内容
与50mL 0.1mol-1 Na2CO3 溶液中 Na+ 的物质的量浓度相同的溶液是( )
| A、50mL 0.2mol?L-1 的 NaCl 溶液 |
| B、100mL 0.1mol?L-1 的 NaCl 溶液 |
| C、25mL 0.2mol?L-1 的 Na2SO4 溶液 |
| D、10mL 0.5mol?L-1 的 Na2CO3 溶液 |
考点:物质的量浓度
专题:物质的量浓度和溶解度专题
分析:电解质溶液离子浓度=电解质浓度×电解质电离产生的该离子的数目,根据碳酸钠化学式可知,碳酸钠溶液中钠离子的浓度为碳酸钠溶液浓度的2倍,所以0.1mol?L-1 Na2CO3 溶液中Na+的钠离子浓度为0.2mol/L,根据选项中各溶质的化学式计算钠离子浓度,进行判断.注意离子的浓度与物质的浓度有关,而与溶液的体积无关.
解答:
解:0.1mol?L-1 Na2CO3 溶液中Na+的钠离子浓度为0.2mol/L.
A、50mL 0.2mol?L-1 的NaCl溶液中钠离子浓度为0.2mol/L,故A正确;
B、100mL 0.1mol?L-1 的NaCl溶液中钠离子浓度为0.1mol/L×1=0.1mol/L,故B错误;
C、25mL0.2mol?L-1的Na2SO4溶液中钠离子浓度为0.2mol/L×2=0.4mol/L,故C错误;
D、10mL0.5mol?L-1的Na2CO3溶液中钠离子的浓度为0.5mol/L×2=1mol/L,故D错误.
故选A.
A、50mL 0.2mol?L-1 的NaCl溶液中钠离子浓度为0.2mol/L,故A正确;
B、100mL 0.1mol?L-1 的NaCl溶液中钠离子浓度为0.1mol/L×1=0.1mol/L,故B错误;
C、25mL0.2mol?L-1的Na2SO4溶液中钠离子浓度为0.2mol/L×2=0.4mol/L,故C错误;
D、10mL0.5mol?L-1的Na2CO3溶液中钠离子的浓度为0.5mol/L×2=1mol/L,故D错误.
故选A.
点评:本题考查物质的量浓度的计算,明确浓度与物质的构成的关系是解答本题的关键,并注意离子的浓度与物质的浓度有关,而与溶液的体积无关.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
当今世界,环境问题日趋严峻,发展“低碳”经济,实现可持续发展已成为人们的共识.下列施可以提高燃料燃烧效率的是①通入适量的空气②提高燃料的着火点③降低燃料的着火点④将煤气化处理⑤将液体燃料化⑥将固体燃料粉碎( )
| A、①④⑤⑥ | B、①②③④ |
| C、③④⑤⑥ | D、②④⑤⑥ |
下列变化需克服相同类型作用力的是( )
| A、氯化钠和金刚石的熔化 |
| B、干冰和C60的熔化 |
| C、氯化氢和氯化钾的溶解 |
| D、溴和汞的气化 |
将13.0g Al、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生气体6.72L(标况).另取等质量的合金溶于过量的稀硝酸中生成6.72L(标况)NO,向反应后的溶液中加入过量的NaOH溶液,得到沉淀的质量是( )
| A、11.85g |
| B、12.7g |
| C、27.45g |
| D、28.3g |
中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700°C时反应制造出纳米级金刚石粉末和另一种化合物.该成果发表在世界权威的《科学》杂志上,被科学家们高度评价为“稻草变黄金”.同学们对此有以下“理解”,你认为其中错误的是( )
| A、该反应可能在空气中进行 |
| B、制造过程中元素种类没有改变 |
| C、另一种化合物是NaCl |
| D、这个反应是置换反应 |
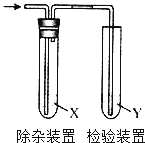 用如图所示装置检验乙烯时不需要除杂的是( )
用如图所示装置检验乙烯时不需要除杂的是( )