题目内容
11.下列鉴别物质的方法能达到目的是( )| A. | 用加热、称重的方法鉴别Na2CO3固体和NaHCO3固体 | |
| B. | 用焰色反应鉴别NaCl固体和NaOH固体 | |
| C. | 某溶液中滴加盐酸能产生无色气体,该气体能使澄清石灰水变浑浊,则原溶液中一定含CO32- | |
| D. | 向某溶液中加入BaCl2溶液出现白色沉淀,再加入HCl溶液,白色沉淀不溶解,则该溶液中肯定有SO42- |
分析 A.碳酸钠稳定,受热不分解,碳酸氢钠受热分解;
B.钠的焰色反应火焰颜色为黄色;
C.二氧化碳和二氧化硫都是能使澄清石灰水变浑浊变浑浊的无色气体;
D.Ba2+和SO42-生成的BaSO4及Ag+与Cl-生成的AgCl均不溶解于水和稀盐酸;
解答 解:A.Na2CO3固体和NaHCO3固体分别加热后,碳酸氢钠受热分解质量变轻,而碳酸钠受热不分解质量不变,可以用加热、称重的方法鉴别两固体,故A正确;
B.焰色反应检验的是某些金属元素的存在,NaCl固体和NaOH固体均存在钠元素,焰色反应时火焰颜色都是黄色,故B错误;
C.能使石灰水变浑浊的气体有二氧化碳和二氧化硫,因此溶液里滴加稀盐酸生成的气体不一定是二氧化碳,溶液里不一定含有CO32-,故C错误;
D.向某溶液中加入BaCl2溶液出现白色沉淀,再加入HCl溶液,白色沉淀不溶解,此沉淀为BaSO4或AgCl,则溶液中不一定有SO42-,故D错误;
故选:A.
点评 考查实验的探究与分析,涉及碳酸盐和碳酸根离子的检验、SO42-的检验及焰色反应原理等,属基础性考查,难度较低.

练习册系列答案
相关题目
19.下列可逆反应达到平衡后,加压或降低温度都可使平衡向逆方向移动的是( )
| A. | 2NO2(g)?N2O4(g)(正反应为放热反应) | |
| B. | 2SO3(g)?2SO2(g)+O2(g)(正反应为吸热反应) | |
| C. | H2(g)+I2(g)?2HI (g)(正反应为放热反应) | |
| D. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g) (正反应为放热反应) |
6.密闭容器中,反应xA(g)+yB(g)?zC(g)达到平衡时,A的浓度为0.5mol•L-1,若保持温度不变,将容器的容积扩大原来的2倍,达到新平衡时,测得A气体的浓度为0.3mol/L,则下列叙述中正确的是( )
| A. | x+y<n | B. | 该化学平衡向正方向移动 | ||
| C. | B的转化率增大 | D. | C的体积分数减小 |
16.下列除杂试剂或方法有错误的是( )
| 原物质 | 所含杂质 | 除杂试剂 | 主要操作方法 | |
| A | HNO3溶液 | H2SO4 | BaCl2溶液 | 过滤 |
| B | CO2 | SO2 | 酸性KMnO4溶液、浓硫酸 | 洗气、干燥 |
| C | SiO2 | Al2O3 | 稀盐酸 | 过滤 |
| D | C2H5OH | CH3COOH | CaO | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
3.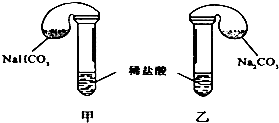 某次化学兴趣小组活动上,三组学生分别用图示甲、乙两装置,探究“NaHCO3和Na2CO3与稀盐酸的反应”,按表中的试剂用量,在相同条件下,将两个气球中的固体粉末同时倒入试管中(装置的气密性已检查) 请回答:
某次化学兴趣小组活动上,三组学生分别用图示甲、乙两装置,探究“NaHCO3和Na2CO3与稀盐酸的反应”,按表中的试剂用量,在相同条件下,将两个气球中的固体粉末同时倒入试管中(装置的气密性已检查) 请回答:
(1)各组反应开始时,甲装置中的气球体积先变大,该装置中反应的离子方程式是HCO3-+H+═H2O+CO2↑.
(2)当试管中不再有气体生成时,三组实验出现不同现象,填写下表的空格.
 某次化学兴趣小组活动上,三组学生分别用图示甲、乙两装置,探究“NaHCO3和Na2CO3与稀盐酸的反应”,按表中的试剂用量,在相同条件下,将两个气球中的固体粉末同时倒入试管中(装置的气密性已检查) 请回答:
某次化学兴趣小组活动上,三组学生分别用图示甲、乙两装置,探究“NaHCO3和Na2CO3与稀盐酸的反应”,按表中的试剂用量,在相同条件下,将两个气球中的固体粉末同时倒入试管中(装置的气密性已检查) 请回答:(1)各组反应开始时,甲装置中的气球体积先变大,该装置中反应的离子方程式是HCO3-+H+═H2O+CO2↑.
(2)当试管中不再有气体生成时,三组实验出现不同现象,填写下表的空格.
| | 试剂用量 | 实验现象 (气球体积变化)) | 分析原因 |
| 第 ① 组 | 42 g NaHCO3 53 g Na2CO3 300mL4 mol/L盐酸 | 甲中气球与乙中 气球的体积相等 | 甲、乙盐酸均过量 n(NaHCO3)=n (Na2CO3) V甲(CO2)=V乙(CO2) |
| 第 ② 组 | 42 g NaHCO3 53 g Na2CO3 300mL3 mol/L盐酸 |
18.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1molNa2O2与SO2完全反应时转移电子数为NA | |
| B. | 18g重水(D2O)所含的电子数为10NA | |
| C. | 0.5molNH4HSO4晶体中,含有H+数目约为0.5 NA | |
| D. | 常温常压下,3gHCHO和CH3COOH的混合物中含有0.4NA个原子 |
 质中含有的化学键类型相同的是( )
质中含有的化学键类型相同的是( )