题目内容
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A、28g乙烯和丁烯的混合物中含有的原子总数为6NA |
| B、标准状况下,22.4L己烷中共价键数目为19NA |
C、1 mol苯乙烯( )中含有的碳碳双键数为4NA )中含有的碳碳双键数为4NA |
| D、15g甲基(-CH3)所含有的电子数是10NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、乙烯和丙烯的最简式为CH2,计算出混合物中含有最简式的物质的量,再计算出含有的原子物质的量;
B、标准状况下己烷不是气体,不能使用标况下的气体摩尔体积计算其物质的量;
C、苯乙烯分子中,苯环中不含有碳碳双键,1mol苯乙烯分子中含有1mol碳碳双键;
D、15g甲基的物质的量为1mol,1mol甲基中含有9mol电子.
B、标准状况下己烷不是气体,不能使用标况下的气体摩尔体积计算其物质的量;
C、苯乙烯分子中,苯环中不含有碳碳双键,1mol苯乙烯分子中含有1mol碳碳双键;
D、15g甲基的物质的量为1mol,1mol甲基中含有9mol电子.
解答:
解:A、28g乙烯和丙烯的混合物中含有2mol最简式CH2,含有6mol原子,含有的原子总数为6NA,故A正确;
B、标况下,己烷不是气体,题中条件无法计算22.4L己烷的物质的量,故B错误;
C、1mol苯乙烯中含有1mol碳碳双键,含有的碳碳双键数为NA,故C错误;
D、15g甲基的物质的量为1mol,含有9mol电子,所含有的电子数是9NA,故D错误;
故选A.
B、标况下,己烷不是气体,题中条件无法计算22.4L己烷的物质的量,故B错误;
C、1mol苯乙烯中含有1mol碳碳双键,含有的碳碳双键数为NA,故C错误;
D、15g甲基的物质的量为1mol,含有9mol电子,所含有的电子数是9NA,故D错误;
故选A.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件;注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.

练习册系列答案
 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案
相关题目
能正确表示四种基本类型反应与氧化反应关系的示意图是( )
A、 |
B、 |
C、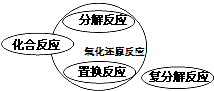 |
D、 |
下列物质充分反应产生的气体体积(标准状况)最大的是( )
| A、100mL 2mol/L的稀硝酸与足量铜充分反应 |
| B、100mL 1mol/L盐酸与足量锌充分反应 |
| C、20mL 10mol/L浓盐酸与足量二氧化锰加热充分反应 |
| D、0.2molCu与足量18.4mol/L浓硫酸加热充分反应 |
实验室中需要配制1mol/L的NaCl溶液448mL,配置时应选用的容量瓶的规格和称取的NaCl质量分别是( )
| A、448mL 26.2g |
| B、500mL 29.3g |
| C、1000mL 29.3g |
| D、450mL 26.2g |
用NA代表阿伏加德罗常数,下列说法正确的是( )
| A、在同温同压时,相同体积的任何气体单质所含的原子数目相同 |
| B、标准状况下,11.2L水所含分子数为0.5NA |
| C、同温同体积时,两种气体的压强比等于物质的量之比 |
| D、46gNO2和N2O4的混合物含有的分子数为NA |
 A、B、C、D、E、X、Y为中学常见的七种物质,它们有如图转化关系(部分产物与反应条件略去):
A、B、C、D、E、X、Y为中学常见的七种物质,它们有如图转化关系(部分产物与反应条件略去):