题目内容
某金属重4g,其原子核外有2mol电子,核内共有1.204×1024个中子,该金属与足量盐酸反应,有0.2mol电子发生转移,生成了6.02×1022个阳离子.该金属的元素符号是 原子核内有 个质子.
考点:质量数与质子数、中子数之间的相互关系
专题:原子组成与结构专题
分析:6.02×1022个阳离子说明金属的物质的量为0.1mol,然后根据
和原子的质子数+中子数=质量数解题.
| m |
| n |
解答:
解:6.02×1022个阳离子说明金属的物质的量为0.1mol,根据
=
=40g/mol,故该元素为Ca,其原子核外有2mol电子,核内共有1.204×1024个中子,质子数和中子数相等,质子数为20,故答案为:Ca;20.
| m |
| n |
| 4 |
| 0.1 |
点评:本题考查学生原子原子中的质子数、中子数以及电子数之间的关系,难度较小,旨在考查学生对基础知识的识记,注意基础知识的积累掌握.

练习册系列答案
相关题目
已知硫铁矿在沸腾炉中燃烧,通入的气体原料为空气,其中N2的体积分数为0.8,则沸腾炉中排除的气体中SO2的体积分数可能是( )
| A、0.13 | B、0.16 |
| C、0.22 | D、0.26 |
下列有关有机物的说法中正确的是( )
| A、符合同一通式的有机物一定互为同系物 |
| B、乙烷不能使溴水和高锰酸钾溶液褪色 |
| C、所有的有机物都很容易燃烧 |
| D、易溶于汽油、酒精、苯等有机溶剂中的物质一定是有机物 |
下列说法正确的是( )
| A、含有离子键和共价键的化合物一定是离子化合物 |
| B、所有元素原子的最外层电子数等于该元素的最高化合价 |
| C、元素的相对原子质量数值上等于该元素的原子序数 |
| D、多电子原子中,在离核较近的区域内运动的电子能量较高 |
 ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨CH3CH2CH(CH3)2 ⑩红磷
⑨CH3CH2CH(CH3)2 ⑩红磷 的系统命名是:
的系统命名是: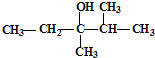 的键线式是
的键线式是 是由一种单体缩聚而成的,该单体的结构简式为
是由一种单体缩聚而成的,该单体的结构简式为