��Ŀ����
�����й�Fe2(SO4)3��Һ��������ȷ����
A������Һ�У�K+��Fe2+��C6H5OH��Br�����Դ�������
B����KI��Һ��Ӧ�����ӷ���ʽ��Fe3+ + 2I��= Fe2+ + I2
C����Ba(OH)2��Һ��Ӧ�����ӷ���ʽ��Fe3+ + SO42��+ Ba2+ + 3OH��= Fe(OH)3��+ BaSO4��
D�� 1L0.1mol/L����Һ��������Zn��ַ�Ӧ������ 11.2gFe
D
��������
���������A�������Ӻͱ��ӷ�����ɫ��Ӧ�����߲��ܴ������棬A����ȷ��B����ɲ��غ㣬Ӧ����2Fe3����2I����2Fe2����I2��B����C����������ȹ�ϵ����ȷ����2Fe3����3SO42����3Ba2����6OH����2Fe(OH)3����3BaSO4����C����D��п�Ľ�����ǿ����������п����������Ӧ�����ӷ���ʽΪ3Zn��2Fe3��=3Zn2����2Fe�������ӵ����ʵ���Ϊ0.2mol����������Zn��Ӧ����0.2mol��������Ϊ0.2mol��56g/mol��11.2g��D��ȷ����ѡD��
���㣺��������������Ӧ�����ӹ����Լ�������й��ж�

��ϰ��ϵ�д�
 ��һ����ͬ���ɽ�����ϵ�д�
��һ����ͬ���ɽ�����ϵ�д� ������Ӧ���ϵ�д�
������Ӧ���ϵ�д� ��ʦ�㾦�ִʾ��ƪϵ�д�
��ʦ�㾦�ִʾ��ƪϵ�д�
�����Ŀ
 CH3OH(g)�����ܱ������г���10 mol CO��20 mol H2��CO��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��
CH3OH(g)�����ܱ������г���10 mol CO��20 mol H2��CO��ƽ��ת�������¶ȡ�ѹǿ�Ĺ�ϵ��ͼ��ʾ��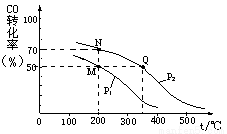
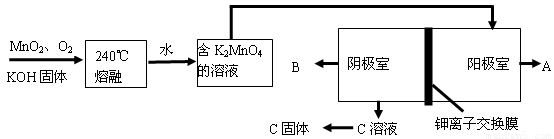
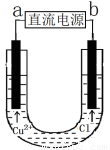
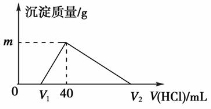
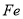 ��ϡ
��ϡ ��ϡ
��ϡ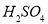 ��Ӧ�������ݲ�����˵��
��Ӧ�������ݲ�����˵�� ��������������û�
��������������û� ��������������Ŀ֮��Ϊ1��1
��������������Ŀ֮��Ϊ1��1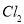 ��
��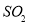 ����ʹƷ����ɫ��˵�����߾���������
����ʹƷ����ɫ��˵�����߾���������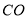 �ܹ����������Ѫ�쵰��ϣ��������ȱ���ж�
�ܹ����������Ѫ�쵰��ϣ��������ȱ���ж�