题目内容
在10L 密闭容器里发生:![]()
![]()
![]() 反应半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率
反应半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率![]() 可表示为
可表示为
A.![]()
B.![]()
C.![]()
D.![]()
C
解析:
化学反应的平均速率是指单位时间内某反应物或生成物浓度的变化量。已知容器的体积为10 L,水蒸气的物质的量的变化量为0.45 mol,则水蒸气物质的量浓度变化量为:
![]()
上述水蒸气浓度的变化时间为半分钟即30g,故用水蒸气表示此反应的速率为:
![]()
再根据同一反应中不同物质的反应速率之比等于化学方程式相应物质的化学计量数之比的规律,即可求出:



很显然,上述用各反应物或生成物表示的平均速率只有选项C是一致的。

 寒假学与练系列答案
寒假学与练系列答案以下是一些物质的熔沸点数据(常压):
|
|
钾 |
钠 |
Na2CO3 |
金刚石 |
石墨 |
|
熔点(℃) |
63.65 |
97.8 |
851 |
3550 |
3850 |
|
沸点(℃) |
774 |
882.9 |
1850(分解产生CO2) |
---- |
4250 |
金属钠和CO2在常压、890℃发生如下反应:
4 Na(g)+ 3CO2(g) 2
Na2CO3(l)+ C(s,金刚石) △H=-1080.9kJ/mol
2
Na2CO3(l)+ C(s,金刚石) △H=-1080.9kJ/mol
(1)上述反应的平衡常数表达式为 ;若4v正(Na)=3v逆(CO2),反应是否达到平衡 (选填“是”或“否”)。
(2)若反应在10L密闭容器、常压下进行,温度由890℃升高到1680℃,若反应时间为10min, 金属钠的物质的量减少了0.20mol,则10min里CO2的平均反应速率为 。
(3)高压下有利于金刚石的制备,理由是 。
(4)由CO2(g)+4Na(g)=2Na2O(s)+C(s,金刚石) △H=-357.5kJ/mol;则Na2O固体与C(金刚石)反应得到Na(g)和液态Na2CO3(l)的热化学方程式 。
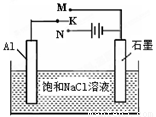
(5)下图开关K接M时,石墨作 极,电极反应式为 。K接N一段时间后测得有0.3mol电子转移,作出y随x变化的图象〖x—代表n(H2O)消耗,y—代表n[Al(OH)3],反应物足量,标明有关数据〗

 (2009?清远模拟)德国人哈伯在1909年发明的合成氨反应原理为:N2(g)+3H2(g)?2NH3(g) 已知298K时:△H=-92.4kJ?mol-1试回答下列问题:
(2009?清远模拟)德国人哈伯在1909年发明的合成氨反应原理为:N2(g)+3H2(g)?2NH3(g) 已知298K时:△H=-92.4kJ?mol-1试回答下列问题:


 反应半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率
反应半分钟后,水蒸气的物质的量增加了0.45mol,则此反应的平均速率 可表示为
可表示为 


