题目内容
14.下列表达式正确的是( )| A. | CH3COOH溶液中CH3COOH的电离:CH3COOH=H ++CH3COO- | |
| B. | 用CuCl2溶液做导电实验,灯泡发光:CuCl2$\frac{\underline{\;电解\;}}{\;}$Cu2++2Cl- | |
| C. | NaHCO3溶液中HCO3-的水解:HCO3-+H2 O?H3 O ++CO32- | |
| D. | 将FeCl3溶液滴入Na2CO3溶液中:2Fe3++3 CO32?+3 H2 O═2Fe(OH)3↓+3 CO2↑ |
分析 A.弱酸在溶液中部分电离;
B.电解CuCl2溶液生成Cu和氯气;
C.HCO3-水解生成碳酸;
D.FeCl3溶液与Na2CO3溶液发生相互促进的水解反应生成氢氧化铁沉淀和二氧化碳气体.
解答 解:A.弱酸在溶液中部分电离,则CH3COOH溶液中CH3COOH的电离:CH3COOH?H++CH3COO-,故A错误;
B.电解CuCl2溶液生成Cu和氯气,所以用CuCl2溶液做导电实验,灯泡发光:CuCl2$\frac{\underline{\;电解\;}}{\;}$Cu+Cl2↑,故B错误;
C.HCO3-水解生成碳酸,则NaHCO3溶液中HCO3-的水解方程式:HCO3-+H2O?OH-+H2CO3,故C错误;
D.FeCl3溶液与Na2CO3溶液发生相互促进的水解反应生成氢氧化铁沉淀和二氧化碳气体,反应的方程式为:2Fe3++3CO32?+3H2O═2Fe(OH)3↓+3CO2↑,故D正确.
故选D.
点评 本题考查了弱电解质的电离和盐的水解,题目侧重于电离方程式和水解方程式书写的考查,题目难度不大,注意把握酸式盐的电离方程式与水解方程式 的区别.

练习册系列答案
相关题目
17. 已知T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表.
已知T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表.
(1)TY2是一种常用的溶剂,是非极性分子(填“极性分子”或“非极性分子”),分子中存在2个σ键.W的最简单氢化物容易液化,理由是氟化氢分子之间存在着氢键.
(2)在25℃、101kPa下,已知13.5g的X固体单质在O2中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为4Al(s)+3 O2(g)=2Al2O3(s)△H=-3352kJ/mol.
(3)基态Y原子中,电子占据的最高能层符号为M;该能层具有的原子轨道数为9、电子数为6.Y、氧、W元素的电负性由大到小的顺序为F>O>S(用元素符号作答).
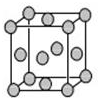
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00g•cm-3,则晶胞边长为$\root{3}{4.72×1{0}^{-23}}$(用含立方根的式子表示);
ZYO4常作电镀液,其中YO42-的空间构型是正四面体,其中Y原子的杂化轨道类型是sp3.Z的单质与人体分泌物中的盐酸以及空气反应可生成超氧酸:
Z+HCl+O2=ZCl+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列说法或表示正确的是AD
A.O2是氧化剂B.HO2是氧化产物
C.HO2在碱中能稳定存在D.1mol Z参加反应有1mol 电子发生转移.
 已知T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表.
已知T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如表.| 元素 | 相关信息 |
| T | T元素可形成自然界硬度最大的单质 |
| W | W与T同周期,核外有一个未成对电子 |
| X | X原子的第一电离能至第四电离能分别是:I1=578kJ•mol-1,I2=1817kJ•mol-1, I3=2745kJ•mol-1,I4=11575kJ•mol-1 |
| Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
| Z | Z的一种同位素的质量数为63,中子数为34 |
(2)在25℃、101kPa下,已知13.5g的X固体单质在O2中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为4Al(s)+3 O2(g)=2Al2O3(s)△H=-3352kJ/mol.
(3)基态Y原子中,电子占据的最高能层符号为M;该能层具有的原子轨道数为9、电子数为6.Y、氧、W元素的电负性由大到小的顺序为F>O>S(用元素符号作答).
(4)已知Z的晶胞结构如图所示,又知Z的密度为9.00g•cm-3,则晶胞边长为$\root{3}{4.72×1{0}^{-23}}$(用含立方根的式子表示);
ZYO4常作电镀液,其中YO42-的空间构型是正四面体,其中Y原子的杂化轨道类型是sp3.Z的单质与人体分泌物中的盐酸以及空气反应可生成超氧酸:
Z+HCl+O2=ZCl+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性.下列说法或表示正确的是AD
A.O2是氧化剂B.HO2是氧化产物
C.HO2在碱中能稳定存在D.1mol Z参加反应有1mol 电子发生转移.
2.天然水因含有Ca2+、Mg2+、HCO3-等离子,煮沸后会形成水垢.现有一种干燥水垢6.32g,加热除去全部结晶水,得到固体M 5.78g;高温灼烧M至恒重,残余固体为CaO和MgO;放出的气体通入足量澄清石灰水中,产生沉淀6.00g;若产生的气体完全被碱石灰吸收,碱石灰增重2.82g.下列推断合理的是( )
| A. | M 中一定不含Mg(OH)2 | B. | M中一定含有MgCO3 | ||
| C. | 5.78 g M中含CaCO30.05mol | D. | 水垢中碳酸盐质量分数为0.823 |
9.用0.1000mol•L-1标准NaOH溶液测定食醋中醋酸的含量,下列说法正确的是( )
| A. | 酸式滴定管、碱式滴定管及锥形瓶均需洗净后再润洗内壁2~3次 | |
| B. | 应该选择酚酞作指示剂 | |
| C. | 滴定过程中眼睛应始终注视滴定管内液面变化 | |
| D. | 读取标准液的刻度时,滴定前平视,滴定后仰视,测定结果偏低 |
19.在已达到电离平衡的0.1mol/L的醋酸溶液中,欲使平衡向电离的方向移动,同时使溶液的pH降低,应采取的措施是( )
| A. | 加少量盐酸 | B. | 加热 | ||
| C. | 加少量醋酸钠晶体 | D. | 加少量NaOH晶体 |
3.关于下列各图的叙述,正确的是( )
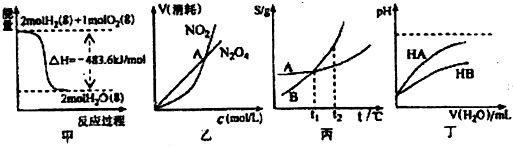

| A. | 甲表示H2与O2发生反应过程中的能量变化,则H2的燃烧热为483.6kJ•mol-l | |
| B. | 乙表示恒温恒容条件下发生的可逆反应2NO2?N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 | |
| C. | 丙表示A、B两物质的溶解度随温度变化情况,将A、B饱和溶液分别由t1℃升温至t2℃时,溶质的质量分数B=A | |
| D. | 丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则同浓度的NaA溶液的pH大于NaB溶液 |
4.常温下,某酸HA溶液和某碱BOH溶液的pH之和为14,两溶液混合后,溶液的pH=7,下列判断中合理的是( )
| 编号 | HA | BOH | 溶液的体积关系 |
| ① | 强酸 | 强碱 | V(HA)<V(BOH) |
| ② | 强酸 | 强碱 | V(HA)=V(BOH) |
| ③ | 强酸 | 弱碱 | V(HA)>V(BOH) |
| ④ | 弱酸 | 强碱 | V(HA)>V(BOH) |
| A. | ①③ | B. | ②③ | C. | ②④ | D. | ①④ |
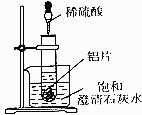 如图所示,把试管放人盛有25℃饱和澄清石灰水的烧杯中,开始往试管中加人若干铝片,再用滴管向试管中加人10mL1mol•L-1稀硫酸.
如图所示,把试管放人盛有25℃饱和澄清石灰水的烧杯中,开始往试管中加人若干铝片,再用滴管向试管中加人10mL1mol•L-1稀硫酸.