题目内容
下列实验能达到实验目的是( )
| A、检验NH4+时,往试样中加入NaOH溶液,微热,用湿润的蓝色石蕊试纸检验逸出的气体 |
| B、向做完蔗糖水解后的溶液中直接加入新制的Cu(OH)2并加热,以检验蔗糖是否水解 |
| C、将混有HCl的CO2通入饱和Na2CO3溶液中除去HCl |
| D、将Al2(SO4)3溶液蒸干制备Al2(SO4)3固体 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.用湿润的红色石蕊试纸检验氨气;
B.蔗糖水解后显酸性,检验葡萄糖应在碱性溶液中;
C.二者均与碳酸钠反应;
D.水解生成硫酸不挥发.
B.蔗糖水解后显酸性,检验葡萄糖应在碱性溶液中;
C.二者均与碳酸钠反应;
D.水解生成硫酸不挥发.
解答:
解:A.用湿润的红色石蕊试纸检验氨气,氨气的检验不合理,故A错误;
B.蔗糖水解后显酸性,检验葡萄糖应在碱性溶液中,则水解后先加碱至碱性再加入新制的Cu(OH)2并加热,以检验蔗糖是否水解,故B错误;
C.二者均与碳酸钠反应,不能除杂,应选饱和碳酸氢钠,故C错误;
D.水解生成硫酸不挥发,则将Al2(SO4)3溶液蒸干制备Al2(SO4)3固体,故D正确;
故选D.
B.蔗糖水解后显酸性,检验葡萄糖应在碱性溶液中,则水解后先加碱至碱性再加入新制的Cu(OH)2并加热,以检验蔗糖是否水解,故B错误;
C.二者均与碳酸钠反应,不能除杂,应选饱和碳酸氢钠,故C错误;
D.水解生成硫酸不挥发,则将Al2(SO4)3溶液蒸干制备Al2(SO4)3固体,故D正确;
故选D.
点评:本题考查化学实验方案的评价,为高频考点,涉及离子和气体的检验、水解及混合物分离提纯、盐类水解等,把握物质的性质及反应原理为解答的关键,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、c(H+)<c(OH-)的溶液中,Na+、K+、SO42-、ClO- |
| B、能使酚酞变红的溶液中:Na+、Cu2+、CO32-、NO3- |
| C、0.1mol?L-1FeCl3溶液中:K+、NH4-、I-、SCN- |
| D、加入铝粉能产生氢气的溶液中:NH4+、Fe2+、NO3-、SO42- |
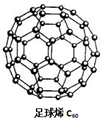 C60可用作储存氢气的材料,结构如图所示.继C60后,科学家又合成了Si60、N60,三种物质结构相似.下列有关说法正确的是( )
C60可用作储存氢气的材料,结构如图所示.继C60后,科学家又合成了Si60、N60,三种物质结构相似.下列有关说法正确的是( )| A、C60、Si60、N60都属于原子晶体 |
| B、C60、Si60、N60分子内共用电子对数目相同 |
| C、由于N-N键能小于N≡N,故N60的稳定性弱于N2 |
| D、由于C-C键长小于Si-Si键,所以C60熔沸点低于Si60 |
室温时,0.01mol?L-1HA溶液的pH=3,向该溶液中逐滴加入NaOH,在滴加过程中,下列有关叙述正确的是( )
| A、原HA溶液中,c(H+)=c(OH-)+c(A-) |
| B、当恰好完全中和时,溶液呈中性 |
| C、当滴入少量的NaOH,促进了HA的电离,溶液的pH升高 |
| D、当NaOH溶液过量时,可能出现:c(A-)>c(Na+)>c(OH-)>c(H+) |
某学生想利用如图装置(烧瓶位置不能移动)收集下列气体:下列操作正确的是( )
 ①H2②Cl2③NH3④O2⑤CH4⑥NO ⑦NO2⑧SO2⑨HCl.
①H2②Cl2③NH3④O2⑤CH4⑥NO ⑦NO2⑧SO2⑨HCl.
 ①H2②Cl2③NH3④O2⑤CH4⑥NO ⑦NO2⑧SO2⑨HCl.
①H2②Cl2③NH3④O2⑤CH4⑥NO ⑦NO2⑧SO2⑨HCl.| A、在烧瓶中充满水,由B进气收集④⑥ |
| B、在烧瓶中充满水,由A进气收集①③⑤⑥⑦ |
| C、烧瓶是干燥的,由B进气收集②④⑥⑦⑧⑨ |
| D、烧瓶是干燥的,由A进气收集①③⑤ |
下列水溶液中能大量共存的一组离子是( )
| A、K+、Al3+、CO32-、Cl- |
| B、Na+、H+、SO42-、SiO32- |
| C、H+、Mg2+、SO42-、I- |
| D、H+、Fe2+、Cl-、NO3- |

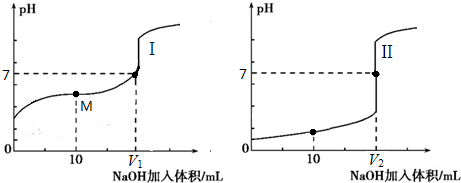 电解质的水溶液中存在电离平衡.
电解质的水溶液中存在电离平衡.