题目内容
19.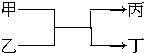 若甲、丙均为短周期,不同主族元素组成的单质,乙、丁都是氧化物,它们之间有如图所示的转化关系,则满足条件的甲和丙可以为( )
若甲、丙均为短周期,不同主族元素组成的单质,乙、丁都是氧化物,它们之间有如图所示的转化关系,则满足条件的甲和丙可以为( )| A. | 碳和镁 | B. | 氟气和氧气 | C. | 碳和氢气 | D. | 氧气和硫 |
分析 甲、乙为短周期不同主族元素组成的单质,乙、丁为氧化物,则该反应是单质和氧化物发生的置换反应,符合甲+丙→乙+丁的置换反应且甲和乙为短周期不同主族的元素形成的单质即可,以此来解答.
解答 解:A.镁和碳是短周期的不同主族元素,发生的反应可以是:2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$C+2MgO,故A选;
B.F、O为短周期不同主族元素,发生氟气与水的反应生成HF和氧气,但HF不是氧化物,故B不选;
C.C、H均为短周期不同主族元素,发生C+H2O$\frac{\underline{\;高温\;}}{\;}$CO+H2,故C选;
D.O、S为同主族元素,发生硫化氢与氧气的置换反应,故D不选;
故选AC.
点评 本题考查无机物的推断,为高频考点,把握元素化合物知识、物质性质及转化、元素在周期表的位置等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
9.设NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1L0.1 mol/L氨水中含有0.1NA NH3分子 | |
| B. | 46gNO2和N2O4混合气体中含有的原子数为3NA | |
| C. | 标准状况下,11.2 L CCl4中含有的分子数为0.5NA | |
| D. | 常温常压下,12g 14C所含原子数为NA |
10.pH是溶液中c(H+)的负对数,若定义pc是溶液中溶质物质的量浓度的负对数,则常温下,某浓度的草酸(H2C2O4)水溶液中pc(H2C2O4)、pc(HC2O4-)、pc(C2O42-)随着溶液pH的变化曲线如图所示:
已知草酸的电离常数K${\;}_{{a}_{1}}$=5.6×10-2,K${\;}_{{a}_{2}}$=5.4×10-5
下列叙述正确的是( )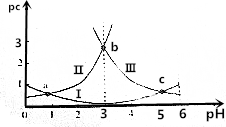
已知草酸的电离常数K${\;}_{{a}_{1}}$=5.6×10-2,K${\;}_{{a}_{2}}$=5.4×10-5
下列叙述正确的是( )

| A. | 曲线Ⅰ表示H2C2O4的变化 | |
| B. | pH=4时,c(HC2O4-)>c(C2O42-) | |
| C. | c(H2C2O4)+c(HC2O4-)+c(C2O42-)在a点和b点一定相等 | |
| D. | 常温下,$\frac{c({H}_{2}{C}_{2}{O}_{4})•c({C}_{2}{{O}_{4}}^{2-})}{{c}^{2}(H{C}_{2}{{O}_{4}}^{-})}$随pH的升高先增大后减小 |
7. 已知下列反应:
已知下列反应:
①2Fe3++2I-?2Fe2++I2(s)(慢)
②I2+2S2O32-═2I-+S4O62-(快)
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的FeCl3溶液,为确保能观察到溶液呈蓝色的现象,S2O32-与Fe3+初始的物质的量需满足的关系为:n(S2O32-):n(Fe3+)<1.
(2)已知Fe3+与I-在水溶液中发生反应①,该反应的正反应速率和I-、Fe3+的浓度关系为v=kcm(I-)•cn(Fe3+)(其中k为常数).
①则该反应①的平衡常数表达式为K=$\frac{{c}^{2}(F{e}^{2+})}{{c}^{2}({I}^{-}){c}^{2}(F{e}^{3+})}$;
②由上表数据可知:I-浓度对反应速率的影响大于Fe3+浓度对反应速率的影响(填“大于”“小于”或“等于”);
③达到平衡后,往反应混合液中加入一定量的CCl4,则上述平衡向右移动(填“向左”、“向右”、“不会”).
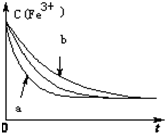
(3)已知反应①在其它条件不变的情况下,只改变一个条件,浓度c(Fe3+)与反应时间t的变化曲线如图所示.则
①曲线a改变的条件是:加入催化剂
②曲线b改变的条件是:降低反应温度
(4)用KSCN溶液检验FeCl3溶液的化学方程式为:FeCl3+3KSCN?Fe(SCN)3(血红色)+3KCl
则达到平衡后下列措施可使溶液颜色变浅的是BC
A.加入少量KCl晶体 B.加入少量Na2SO3晶体
C.加入少量Na2CO3溶液 D.加入较浓的KSCN溶液
(5)已知25℃时,Ksp[Fe(OH)3]=2.79×10-39,Kw=1×10-14,则该温度下反应:Fe (OH)3+3H+?Fe3++3H2O达平衡时$\frac{c(F{e}^{3+})}{{c}^{3}({H}^{+})}$=2.79×103.
 已知下列反应:
已知下列反应:①2Fe3++2I-?2Fe2++I2(s)(慢)
②I2+2S2O32-═2I-+S4O62-(快)
(1)向KI、Na2S2O3与淀粉的混合溶液中加入一定量的FeCl3溶液,为确保能观察到溶液呈蓝色的现象,S2O32-与Fe3+初始的物质的量需满足的关系为:n(S2O32-):n(Fe3+)<1.
(2)已知Fe3+与I-在水溶液中发生反应①,该反应的正反应速率和I-、Fe3+的浓度关系为v=kcm(I-)•cn(Fe3+)(其中k为常数).
| cm(I-)(mol/L)m | cn(Fe3+)[(mol/L)n] | v[mol/(L•s)] | |
| a | 0.20 | 0.80 | 0.032 |
| b | 0.60 | 0.40 | 0.144 |
| c | 0.80 | 0.20 | 0.128 |
②由上表数据可知:I-浓度对反应速率的影响大于Fe3+浓度对反应速率的影响(填“大于”“小于”或“等于”);
③达到平衡后,往反应混合液中加入一定量的CCl4,则上述平衡向右移动(填“向左”、“向右”、“不会”).
(3)已知反应①在其它条件不变的情况下,只改变一个条件,浓度c(Fe3+)与反应时间t的变化曲线如图所示.则
①曲线a改变的条件是:加入催化剂
②曲线b改变的条件是:降低反应温度
(4)用KSCN溶液检验FeCl3溶液的化学方程式为:FeCl3+3KSCN?Fe(SCN)3(血红色)+3KCl
则达到平衡后下列措施可使溶液颜色变浅的是BC
A.加入少量KCl晶体 B.加入少量Na2SO3晶体
C.加入少量Na2CO3溶液 D.加入较浓的KSCN溶液
(5)已知25℃时,Ksp[Fe(OH)3]=2.79×10-39,Kw=1×10-14,则该温度下反应:Fe (OH)3+3H+?Fe3++3H2O达平衡时$\frac{c(F{e}^{3+})}{{c}^{3}({H}^{+})}$=2.79×103.
4.下列各组物质中互为同分异构体的是( )
| A. | 葡萄糖和蔗糖 | B. | 蔗糖和麦芽糖 | ||
| C. | 甲酸甲酯(HCOOCH3)和乙酸(CH3COOH) | D. | 淀粉和纤维素 |
11.法国里昂的科学家最近发现一种由四个中子构成的粒子,这种粒子为“四中子”,也有人称之为“零号元素”.下列有关“四中子”粒子的说法正确的是( )
| A. | 该粒子不显电性 | |
| B. | 该粒子的质量数与${\;}_{z}^{4}$He的相同,两者互为同位素 | |
| C. | 在元素周期表中与氢元素占同一位置 | |
| D. | 1mol该粒子的质量为8g |
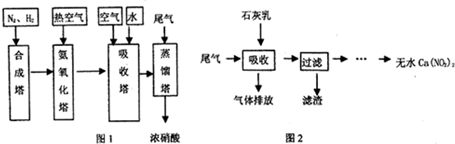
 CO+3H2. 在原料气制备过程中混有的CO对催化剂有毒害作用,欲除去原料气中的CO,可通过反应CO(g)+H2O(g)?CO2(g)+H2(g)来实现.己知1100K时该反应的平衡常数K=0.64,若要使CO的转化率超过80%,则起始物中c(H2O):c(CO)不低于5.8:1.
CO+3H2. 在原料气制备过程中混有的CO对催化剂有毒害作用,欲除去原料气中的CO,可通过反应CO(g)+H2O(g)?CO2(g)+H2(g)来实现.己知1100K时该反应的平衡常数K=0.64,若要使CO的转化率超过80%,则起始物中c(H2O):c(CO)不低于5.8:1. 6xH2O+(2x+3)N2.
6xH2O+(2x+3)N2.
 在如图所示的物质转化关系中(部分反应条件及产物省略),化合物A由短周期元素组成,所含离子数目比为1:2;B是常见的无色液体,C是能使湿润的红色石蕊试纸变蓝色的气体,E是淡黄色粉末,D、F、G均为无色气体.
在如图所示的物质转化关系中(部分反应条件及产物省略),化合物A由短周期元素组成,所含离子数目比为1:2;B是常见的无色液体,C是能使湿润的红色石蕊试纸变蓝色的气体,E是淡黄色粉末,D、F、G均为无色气体.