题目内容
MnO2+4HCl(浓)=MnCl2+Cl2↑+2H2O
(1) 该反应中HCl作 _________剂,Cl2为_________产物,4 mol HCl中有_________mol生成Cl2,另外__________mol HCl生成MnCl2。
(2) 我们把生成盐的酸所起的作用称为酸性,则起酸性作用的HCl与发生氧化还原反应的HCl的物质的量之比为_____________。
(2)1:1

 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案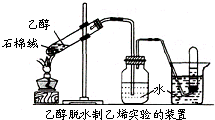 中新社2008年10月30日报道,在从日本进口的日式酱油、芥末酱中检测出了甲苯和乙酸乙酯.试回答下列问题:
中新社2008年10月30日报道,在从日本进口的日式酱油、芥末酱中检测出了甲苯和乙酸乙酯.试回答下列问题:(1)下列有关甲苯的说法不正确的是
A.甲苯和苯互为同系物
B.甲苯主要是从石油中分离获得
C.甲苯在一定条件下能发生取代、加成及氧化反应
D.为了让油漆中的甲苯等有毒物质散逸,新装璜的住房应开窗充分通风
(2)工业上常以乙醇为唯一原料一步制取乙酸乙酯,该反应的化学方程式为
(3)某学习小组拟探究实验室制乙烯,试回答下列问题.
①实验室常用乙醇在浓硫酸作用下脱水制取乙烯,该反应的化学方程式为
②上述反应以浓硫酸为催化剂,可能出现的问题有
③下表是某次探究实验现象记载.据表可知,探究实验中反应最合适的催化剂及反应温度分别是
| 催化剂 | ①浓硫酸 | ②石棉绒 (闪石) |
③P2O5 | ④浓硫酸 石棉绒 |
⑤P2O5 石棉绒 |
| KMnO4/H+褪色情况 | 褪色 | 几乎不褪色 | 褪色 | 褪色 | 褪色 |
| 加热产生气体的时间 | 45s | 50s | 35s | 47s | 38s |
| 反应温度 | 170℃ | 180℃ | 82℃ | 170℃ | 87℃ |
| 气体气流量 | 多 | 很少 | 多 | 较多 | 较多 |
| 反应液炭化情况 | 严重 | 无炭化 | 无炭化 | 严重 | 无炭化 |
A.生物质能是一种洁净、可再生能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式_________________________。
(2)根据等电子原理,写出CO分子的结构式______________________。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是_____________________;甲醛分子中碳原子轨道的杂化类型为_____________________。
②甲醛分子的空间构型是_____________________;1 mol甲醛分子中σ键的数目为_____________________。

③在1个Cu2O晶胞中(结构如图所示),所包含的Cu原子数目为_____________________。
B.环己酮是一种重要的化工原料,实验室常用下列方法制备环己酮:

环己醇、环己酮和水的部分物理性质见下表:
物质 | 沸点(℃) | 密度(g·cm-3, | 溶解性 |
环己醇 | 161.1(97.8)* | 0.962 4 | 能溶于水 |
环己酮 | 155.6(95)* | 0.947 8 | 微溶于水 |
水 | 100.0 | 0.998 2 |
|
*括号中的数据表示该有机物与水形成的具有固定组成的混合物的沸点
(1)酸性Na2Cr2O7溶液氧化环己醇反应的ΔH<0,反应剧烈将导致体系温度迅速上升,副反应增多。实验中将酸性Na2Cr2O7溶液加到盛有环己醇的烧瓶中,在55~
①酸性Na2Cr2O7溶液的加料方式为_____________________。
②蒸馏不能分离环己酮和水的原因是_____________________。
(2)环己酮的提纯需要经过以下一系列的操作:a.蒸馏,收集151~
①上述操作的正确顺序是_______________________(填字母)。
②上述操作b、c中使用的玻璃仪器除烧杯、锥形瓶、玻璃棒外,还需_______________。
③在上述操作c中,加入NaCl固体的作用是_______________________________________
______________________________________________________________________________。
(3)利用核磁共振氢谱可以鉴定制备的产物是否为环己酮,环己酮分子中有______________种不同化学环境的氢原子。



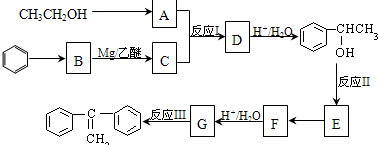
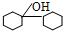 是合成药物中的常用物质,实验室可以用环己烯为原料,其它无机试剂任选,合成该有机物:_____
是合成药物中的常用物质,实验室可以用环己烯为原料,其它无机试剂任选,合成该有机物:_____