题目内容
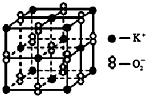 高温下,超氧化钾晶体(KO2)呈立方体结构(与NaCl晶体结构相似).如图为超氧化钾晶体的一个晶胞.则有关下列说法不正确的是( )
高温下,超氧化钾晶体(KO2)呈立方体结构(与NaCl晶体结构相似).如图为超氧化钾晶体的一个晶胞.则有关下列说法不正确的是( )| A、KO2中既存在离子键也存在共价键 |
| B、一个KO2晶胞中摊得的K+和O2-粒子数均为4个 |
| C、晶体中与每个K+距离最近的O2-有8个 |
| D、与K+距离相等且最近的K+有12个 |
考点:晶胞的计算
专题:化学键与晶体结构
分析:A.根据晶体组成微粒判断;
B.根据均摊法计算;
C、由晶胞图可知,晶体中与每个K+距离最近的O2-有6个;
D.由晶胞图可知,晶体中与每个K+距离最近的K+有12个;
B.根据均摊法计算;
C、由晶胞图可知,晶体中与每个K+距离最近的O2-有6个;
D.由晶胞图可知,晶体中与每个K+距离最近的K+有12个;
解答:
A.K+离子与O2-离子形成离子键,O2-离子中O原子间形成共价键,故A正确;
B.K+离子位于顶点和面心,数目为8×
+6×
=4,O2-离子位于棱心和体心,数目为12×
+1=4,即每个晶胞中含有4个K+和4个O2-,故B正确;
C、由晶胞图可知,以晶胞上方面心的K+离子为研究对象,其平面上与其距离最近的O2-有4,上方和下方各有一个,共有6个,故C错误;
D.由晶胞图可知,晶体中与每个K+距离最近的K+有12个,故D正确;
故选C.
B.K+离子位于顶点和面心,数目为8×
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 4 |
C、由晶胞图可知,以晶胞上方面心的K+离子为研究对象,其平面上与其距离最近的O2-有4,上方和下方各有一个,共有6个,故C错误;
D.由晶胞图可知,晶体中与每个K+距离最近的K+有12个,故D正确;
故选C.
点评:本题考查晶胞结构计算、微粒间作用力,难度不大,要有一定的空间想象力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
现行空气质量日报中,未计入空气污染指数项目的是( )
| A、SO2 |
| B、NO2 |
| C、CO2 |
| D、可吸入颗粒物 |
有关水的电解实验,下列说法正确的是( )
| A、正、负极产生的气体质量比是1:2 |
| B、证明了水是由氢气和氧气组成 |
| C、与电源正极相连的一端产生氢气 |
| D、水能电解说明了分子是可分的 |
下列说法正确的是( )
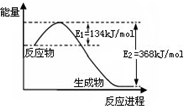

| A、已知1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化如图,则NO2和CO反应的热化学方程式为:NO2(g)+CO(g)=CO2(g)+NO(g);△H=+234 kJ?mol-1 |
| B、氯化铵溶液中加入足量的过氧化钠,仅产生一种气体 |
| C、25℃时,0.10 mol?L-1 NaHCO3溶液,加水稀释后,c(H+)与c(OH-)的乘积变小 |
| D、常温下,反应2A(s)+B(g)=2C(g)+D(g)不能自发进行,则该反应△H一定大于0 |
下列物质转化关系中,需要加入氧化剂才能实现的是( )
| A、Na2O2→O2 |
| B、MnO4-→Mn2+ |
| C、Fe2+→Fe3+ |
| D、CO2→HCO3- |
下列物质的名称、俗名与化学式完全对应的是( )
| A、氯化钠 食盐 NaCl2 |
| B、碳酸氢钠 纯碱 NaHCO3 |
| C、氢氧化钙 熟石灰 CaO |
| D、氢氧化钠 烧碱 NaOH |
能正确表示下列反应的离子方程式是( )
| A、醋酸钠的水解反应:CH3COO-+H3O+=CH3COOH+H2O |
| B、碳酸氢钙与过量的NaOH溶液反应:Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
| C、向FeBr2溶液中通入过量氯气:2Fe2++Cl2═2Fe3++2Cl- |
| D、稀硝酸与过量的铁屑反应:3Fe+8H++2NO3-=3Fe3++2NO↑+4H2O |
我们食用的大豆最终水解、补充给人体的主要成分是( )
| A、氨基酸 | B、糖类 |
| C、蛋白质 | D、油脂 |
在容积固定的密闭容器中发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g),700℃时平衡常数为1.47,900℃时平衡常数为2.15.下列说法正确的是( )
| A、从700℃到900℃,平衡体系中气体的密度变大 | ||
B、该反应的化学平衡常数表达式为K=
| ||
| C、绝热容器中进行该反应,温度不再变化,则达到化学平衡状态 | ||
| D、该反应的正反应是放热反应 |