题目内容
5.氮族元素(Nitrogen group)是元素周期表VA 族的所有元素,包括氮(N)、磷(P)、砷(As)、锑(Sb)、铋(Bi)和Uup共计六种.(1)氮族元素的外围电子排布式的通式为ns2np3;基态磷原子中,电子占据的最高能层符号为M,该能层具有的原子轨道数为9.
(2)PH3分子的VSEPR模型为四面体形,键角NH3>H2O(填“>”、“<”或“=”).
(3)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子中氮的杂化方式为sp.
(4)从化合物NF3和NH3的结构与性质关系比较,回答它们两者如下性质差异原因:
①NF3的沸点为-129℃,而NH3的沸点为-33℃,其原因是NH3能形成氢键,NF3只有范德华力.
②NH3易与Cu2+反应,而NF3却不能,其原因是F的电负性大于N元素,NF3中N-F成键电子对偏向于F原子,N原子上的孤对电子难与铜离子形成配离子.
(5)磷化硼是一种受到高度关注的耐磨涂料,它可用作金属的表面保护层,磷化硼晶体的晶胞结构与金刚石类似,磷原子作面心立方最密堆积,则硼原子的配位数为4;已知磷化硼的晶胞边长a=478pm,计算晶体中硼原子和磷原子的核间距(dB-P)=207pm(保留三位有效数字).
分析 (1)氮族元素的外围电子为其最外层上s、p能级电子;基态磷原子中,电子占据的最高能层符号为M,该能层有1个s轨道、3个p轨道、5个d轨道;
(2)PH3分子中P原子价层电子对个数是4且含有一个孤电子对,根据价层电子对互斥理论判断该分子的VSEPR模型,成键电子对和孤电子对之间的排斥力小于孤电子对之间的排斥力,据此判断键角;
(3)氮的最高价氧化物为N2O5,由两种离子构成,其中阴离子构型为平面正三角形,化学式应为NO3-,则其阳离子的化学式为:NO2+,根据价层电子对互斥理论判断原子杂化方式;
(4)①分子晶体中分子间含有氢键的物质熔沸点较高;
②NF3中N-F成键电子对偏向于F原子,N原子上的孤对电子难与铜离子形成配离子;
(5)磷化硼结构如图所示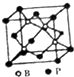 ,该晶胞中B原子为4个、P原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,每个P原子连接4个B原子,每个B原子连接4个P原子,则硼原子的配位数为4;晶体中硼原子和磷原子的核间距(dB-P)等该晶胞体对角线的$\frac{1}{4}$,据此计算.
,该晶胞中B原子为4个、P原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,每个P原子连接4个B原子,每个B原子连接4个P原子,则硼原子的配位数为4;晶体中硼原子和磷原子的核间距(dB-P)等该晶胞体对角线的$\frac{1}{4}$,据此计算.
解答 解:(1)氮族元素的外围电子为其最外层上s、p能级电子,则氮族元素外围电子排布式为ns2np3;
基态磷原子中,电子占据的最高能层符号为M,该能层有1个s轨道、3个p轨道、5个d轨道,所以有9个轨道,
故答案为:ns2np3;M;9;
(2)PH3分子中P原子价层电子对个数是4且含有一个孤电子对,根据价层电子对互斥理论判断该分子的VSEPR模型为四面体形,成键电子对和孤电子对之间的排斥力小于孤电子对之间的排斥力,氨气分子中只含一个孤电子对、水分子中含有两个孤电子对,所以键角NH3>H2O,
故答案为:四面体形;>;
(3)氮的最高价氧化物为N2O5,由两种离子构成,其中阴离子构型为平面正三角形,化学式应为NO3-,则其阳离子的化学式为:NO2+,其中心原子价电子对数为$\frac{5-1}{2}$=2,根据价层电子对互斥理论判断原子杂化方式为sp,
故答案为:sp;
(4)①NH3分子间存在氢键,作用力大,而NF3只存在分子间作用力,两种作用力前者较强,物质的沸点较高,
故答案为:NH3能形成氢键,NF3只有范德华力;
②F的电负性大于N元素,NF3中N-F成键电子对偏向于F原子,N原子上的孤对电子难与铜离子形成配离子,所以NF3不易与Cu2+形成配离子,
故答案为:F的电负性大于N元素,NF3中N-F成键电子对偏向于F原子,N原子上的孤对电子难与铜离子形成配离子;
(5)磷化硼结构如图所示 ,该晶胞中B原子为4个、P原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,每个P原子连接4个B原子,每个B原子连接4个P原子,则硼原子的配位数为4,晶体中硼原子和磷原子的核间距(dB-P)等该晶胞体对角线的$\frac{1}{4}$=$\frac{1}{4}\sqrt{3}$a=$\frac{1}{4}\sqrt{3}$×478pm=207pm,
,该晶胞中B原子为4个、P原子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,每个P原子连接4个B原子,每个B原子连接4个P原子,则硼原子的配位数为4,晶体中硼原子和磷原子的核间距(dB-P)等该晶胞体对角线的$\frac{1}{4}$=$\frac{1}{4}\sqrt{3}$a=$\frac{1}{4}\sqrt{3}$×478pm=207pm,
故答案为:207.
点评 本题考查物质结构和性质,为高频考点,涉及晶胞计算、氢键、键角、微粒空间构型、原子核外电子排布等知识点,侧重考查学生知识应用、计算、空间想象能力,难点是晶胞计算,注意该晶胞中B-P原子核间距与体长关系,题目难度中等.

 名校课堂系列答案
名校课堂系列答案| A. | ②③⑤⑥⑦ | B. | ③④⑤⑥⑦ | C. | ①②③⑤⑦⑥ | D. | ①③⑤⑥⑦ |
| A. | 羟基的电子式: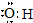 | |
| B. | 过氧化氢的电子式: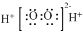 | |
| C. | As的原子的特征电子排布式:[Ar]4s14p3 | |
| D. | 基态Mg原子的核外电子排布图: |
| A. | 1 L水中含有1 mol NaCl | |
| B. | 溶液中含有1 mol NaCl | |
| C. | 1 L溶液中含有1 molNaCl | |
| D. | 将58.5 g NaCl溶于1 L水中所得的溶液 |
| A. | 至少存在4种离子 | |
| B. | Cl-一定存在,且c(Cl )≥0.4 mol/L | |
| C. | SO42-、NH4+,一定存在,Cl-可能不存在 | |
| D. | CO32-、Al3+一定不存在,K+可能存在 |
 材料的开发、应用和发展是科技进步的结果,同时,材料的发展也促进了科技的进步和发展.
材料的开发、应用和发展是科技进步的结果,同时,材料的发展也促进了科技的进步和发展.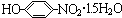 .
.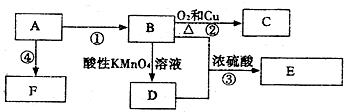
 ,C的名称乙醛,
,C的名称乙醛,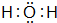 、
、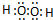 ,D、E形成的化合物
,D、E形成的化合物 .
.