题目内容
18.下列物质中,不能用于生活污水的净化的是( )| A. | 明矾 | B. | 氯化铁 | C. | 硫酸铝 | D. | 氯化钠 |
分析 明矾、氯化铁、硫酸铝等试剂中电离出阳离子能够水解生成胶体,胶体粒子具有较大吸附面积,从而能够净水,而氯化钠中氯离子和钠离子都无法净化生活污水.
解答 解:A.明矾电离出的铝离子水解生成氢氧化铝胶体,氢氧化铝胶粒具有吸附性,可将小颗粒泥尘聚集成大颗粒,有利于沉降,从而起到净水效果,故A不选;
B.氯化铁电离出的铁水解生成氢氧化铝胶体,氢氧化铝胶粒具有吸附性,可起到净水作用,故B不选;
C.硫酸铝电离出的铝离子水解生成氢氧化铝胶体,氢氧化铝胶粒具有较大表面积,可吸附污水中的小颗粒,从而起到净水效果,故C不选;
D.NaCl在水中电离出的钠离子和氯离子不会水解,也不具有强氧化性,无法净化污水,故D选;
故选D.
点评 本题考查了生活污水的净化原理,题目难度不大,明确常见元素及其化合物性质为解答关键,注意掌握常见污水净化方法,试题有利于提高学生的灵活应用能力.

练习册系列答案
相关题目
6.含有6.02×1023个O原子的H3PO4的物质的量是( )
| A. | 1 mol | B. | 0.5 mot | C. | 0.25 mol | D. | 0.125 mol |
13.下列实验操作正确的是( )
| A. | 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 | |
| B. | 蒸馏操作时,应使温度计水银球插入蒸馏烧瓶内的液面以下 | |
| C. | 用蒸发的方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干 | |
| D. | 用滴管滴加液体时滴管应垂直悬垂在容器上方且不能触及容器内壁 |
10.与OHCCH2CH2CHO互为同系物且相对分子质量比其大28的同分异构体有( )
| A. | 5种 | B. | 7种 | C. | 9种 | D. | 11种 |
1.以粗氧化锌粉(含FeO、Fe2O3、ZnS等)制取活性ZnO的工艺如下:
步骤1:以H2SO4浸出粗氧化锌,同时加入H2O2;
步骤2:过滤,调节滤液的pH;
步骤3:过滤,向滤液中加NH4HCO3,得碱式碳酸锌沉淀;
步骤4:过滤、洗涤、煅烧,得产品.
已知:离子沉淀的pH见下表.
(1)加入H2O2时能浸出硫化锌,同时生成淡黄色固体,写出其化学方程式ZnS+H2O2+H2SO4=ZnSO4+2H2O+S.
(2)步骤2中调节溶液pH的范围是3.7~5.4.
(3)取洗涤、干燥后的碱式碳酸锌68.2g,充分灼烧后测得残留物质的质量为48.6g,将所得气体通入足量澄清石灰水中,得沉淀20g.计算碱式碳酸锌的组成(用化学式表示,写出计算过程).ZnCO3•2Zn(OH)2•H2O 或Zn3(OH)4CO3•H2O.
步骤1:以H2SO4浸出粗氧化锌,同时加入H2O2;
步骤2:过滤,调节滤液的pH;
步骤3:过滤,向滤液中加NH4HCO3,得碱式碳酸锌沉淀;
步骤4:过滤、洗涤、煅烧,得产品.
已知:离子沉淀的pH见下表.
| 离子 | 开始沉淀pH | 沉淀完全pH |
| Fe2+ | 7.6 | 9.6 |
| Fe3+ | 2.7 | 3.7 |
| Zn2+ | 5.4 | 8.0 |
(2)步骤2中调节溶液pH的范围是3.7~5.4.
(3)取洗涤、干燥后的碱式碳酸锌68.2g,充分灼烧后测得残留物质的质量为48.6g,将所得气体通入足量澄清石灰水中,得沉淀20g.计算碱式碳酸锌的组成(用化学式表示,写出计算过程).ZnCO3•2Zn(OH)2•H2O 或Zn3(OH)4CO3•H2O.
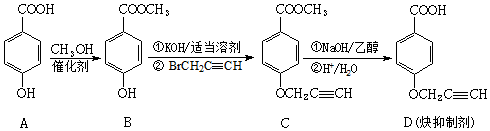
 (中的一种).
(中的一种).