题目内容
在水溶液中能大量共存,且加入过量稀硫酸时,有气体生成的是( )
| A、Na+、Ag+、CO32-、Cl- |
| B、K+、Ba2+、SO42-、Cl- |
| C、Na+、K+、CO32-、Cl- |
| D、H+、K+、Cl-、HCO3- |
考点:离子共存问题
专题:离子反应专题
分析:根据离子之间不能结合生成沉淀、气体、水等,则能大量共存,并加入过量稀硫酸时有气体生成来解答.
解答:
解:A.Ag+分别与CO32-、Cl-结合生成沉淀,不能大量共存,故A错误;
B.Ba2+、SO42-结合生成沉淀,不能大量共存,故B错误;
C.该组离子之间不反应,可大量共存,且加硫酸与CO32-反应生成气体,故C正确;
D.H+、HCO3-结合生成水和气体,不能大量共存,故D错误;
故选C.
B.Ba2+、SO42-结合生成沉淀,不能大量共存,故B错误;
C.该组离子之间不反应,可大量共存,且加硫酸与CO32-反应生成气体,故C正确;
D.H+、HCO3-结合生成水和气体,不能大量共存,故D错误;
故选C.
点评:本题考查离子的共存,为高频考点,把握习题中的信息及常见离子之间的反应为解答的关键,侧重复分解反应的考查,题目难度不大.

练习册系列答案
相关题目
一定温度下可逆反应:A(s)+2B(g)?2C(g)+D(g);△H>0.现将1molA和2molB加入甲容器中,将4molC和2mol D加入乙容器中,此时控制活塞P,使乙的容积为甲的2倍,t1时两容器内均达到平衡状态(如图1所示,隔板K不能移动).下列说法正确的是( )


| A、保持温度和活塞位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的度的2倍 |
| B、保持活塞位置不变,升高温度,达到新的平衡后,甲、乙中B的体积分数均增加 |
| C、保持温度不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数是甲中C的体积分数的2倍 |
| D、保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )
A、NH4Cl
| ||||
| B、NH3+CO2+H2O═NH4HCO3 | ||||
| C、2NaOH+Cl2═NaCl+NaClO+H2O | ||||
| D、2Na2O2+2CO2═2Na2CO3+O2 |
下列有关实验原理、方法和结论都正确的是( )
| A、向相同浓度的NaBr、NaI溶液中滴加硝酸银溶液,先出现黄色沉淀,说明KSP (AgI)>KSP (AgBr) |
| B、在3mL苯酚溶液中滴入几滴溴水,没有沉淀生成,说明苯酚没有和溴水反应 |
| C、向某有机物中加入氢氧化钠溶液、加热,然后向其中加入硝酸银溶液,发现产生了白色沉淀,说明该有机物中含有氯元素 |
| D、室温下向苯和少量苯酚的混合溶液中加入适量NaOH溶液,振荡、静置后分液,可除去苯中少量苯酚 |
下列各组离子在相应的条件下能大量共存的是( )
| A、在c(H+)/c(OH-)=1×10-14的溶液中:NH4+、Ca2+、Cl-、K+ |
| B、水电离的c(H+)=10-13mol?L-1的溶液中:Fe3+、SO42-、K+、SCN- |
| C、在c(H+)=10-14mol/L的溶液中可能含:Na+,AlO22-,CO32-,SO32- |
| D、c(OH-)=1×10-14mol/L的溶液中:Na+、K+、Cl-、S2O32- |
下列各对物质中属于同系物的是( )
A、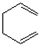 与 与 |
B、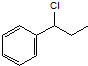 与 与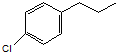 |
| C、石墨与足球烯 |
D、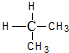 与 与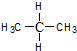 |