题目内容
11.NO2、NH3、O2混合气体共1.2mol,通过稀硫酸后溶液质量增加45g,气体体积缩小为2.24L(标况),将带火星的木条插入其中,木条不复燃,原混合气体的平均相对分子质量为( )| A. | 46 | B. | 40 | C. | 37.5 | D. | 17 |
分析 根据混合气体所发生的反应:氨气与稀硫酸溶液发生反应、NO2和O2在溶液中发生反应结合公式n=$\frac{V}{{V}_{m}}$进行计算.
解答 解:氨气与稀硫酸溶液发生如下反应:2NH3+H2SO4=(NH4)2SO4(若氨气过量,则过量的氨气会溶于水);NO2和O2在溶液中发生如下反应:3NO2+H2O=2HNO3+NO;2NO+O2=2NO2;将两个反应方程式相加可得总反应方程式:O2+4NO2+2H2O=4HNO3(此反应仅用于计算)由质量守恒定律可得:溶液增加的质量为溶解的气体的质量,所以溶液增加的质量加剩余气体的质量为原混合气体的质量,带火星的木头不复燃说明氧气充分反应,则剩余的2.24L气体为NO;剩余气体的物质的量为n=$\frac{V}{{V}_{m}}$=$\frac{2.24L}{22.4L/mol}$=0.1mol;,则剩余的NO的质量为m=n×M=0.1mol×30g/mol=3g,所以原混合气体的质量为3g+45g=48g,所以原混合气体的平均摩尔质量M=$\frac{m}{n}$=$\frac{48g}{1.2mol}$=40g/mol.
综上所述结合选项,则得出结论:原混合气体的平均相对分子质量为40(摩尔质量在数值上等于相对分子质量).
故选B.
点评 本题是一道平均分子量的计算题,考查学生分析和解决问题的能力,综合性较强,难度较大.

练习册系列答案
相关题目
2.下列说法中,正确的是( )
| A. | 干冰升华时要吸收热量,所以这是吸热反应 | |
| B. | 化学反应中能量的变化都表现为热量的变化 | |
| C. | 1 mol Ba(OH)2与1 mol H2SO4反应释放的热量为Q,则Q为它们反 应的中和热 | |
| D. | 物质燃烧可看成“储存”在物质内部的能量(化学能)转化为热能 释放出来 |
19.下列分子式表示的有机物中,含单官能团的同分异构体数目最多的是( )
| A. | C4H8 | B. | C4H7Cl | C. | C4H8O | D. | C4H10O |
6.下列有关实验操作的叙述中正确的是( )
| A. | 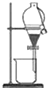 用于分离水和乙醇的混合物 | |
| B. | 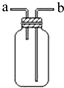 可用于H2,NH3,CO2,Cl2,HCl,NO2等气体收集 | |
| C. | 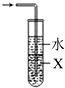 当X选用苯时可进行NH3和HCl的吸收,并防止倒吸 | |
| D. | 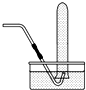 常用于实验室收集氧气、氢气等 |
3.下列有关平衡常数的说法正确的是( )
| A. | 将某浓度氢氟酸溶液升高温度,氢氟酸的电离平衡常数Ka将变小 | |
| B. | 常温下,向纯水中加入碳酸钠,水的电离程程度变大,Kw变大 | |
| C. | 化学平衡常数K与温度有关,随温度的升高,K可能增大也可能减小,或者不变 | |
| D. | 已知,K=$\frac{{c}^{2}(C{O}_{2})•{c}^{6}({H}_{2})}{{c}^{3}({H}_{2}O)•c(C{H}_{3}C{H}_{2}OH)}$则对应的化学反应可以表示为:CH3CH2OH(g)+3H2O(g)?2CO2( g)+6H2(g) |
20.下列有关元素周期表的说法中不正确的是( )
| A. | 氢处于第一周期 | B. | 第三周期元素全部是金属元素 | ||
| C. | 第二周期共有8种元素 | D. | 氯处于VⅡA族 |
