题目内容
16.一定条件下,向容器的体积为4L的密闭容器中通入1molN2和3molH2,发生反应:N2(g)+3H2(g)?2NH3(g)△H<0,达到平衡后.试回答下列问题:(1)该条件下,反应的平衡常数表达式K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$.达到平衡后,若其它条件不变,升高体系的温度,平衡常数K将减小(填“增大”、“减小”或“不变”下同).
(2)达到平衡后,在恒容条件下,向容器中通入氦气(He),氮气的转化率将不变.
分析 (1)化学平衡常数等于生成物浓度幂之积与反应物浓度幂之积的比值;升高温度,平衡逆向移动;
(2)通入惰性气体,平衡不移动,以此解答该题.
解答 解:(1)对于N2(g)+3H2(g)?2NH3(g),K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$,升高温度,平衡逆向移动,则平衡常数K将减小,
故答案为:$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})•{c}^{3}({H}_{2})}$;减小;
(2)在恒容条件下,通入惰性气体,平衡不移动,氮气的转化率不变,故答案为:不变.
点评 本题考查化学平衡的影响因素以及化学平衡常数问题,为高频考点,侧重考查学生的分析能力,注意把握浓度、温度、稀有气体对反应的影响,明确可逆反应的特点及平衡常数只与温度有关,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.90%的硫酸与10%的硫酸等体积混合,所得溶液的质量分数为( )
| A. | 等于50% | B. | 大于50% | C. | 小于50% | D. | 无法确定 |
4.设NA为阿伏加德罗常数,下列叙述错误的是( )
| A. | 标况下,4.48L氦气和重氢气的混合物中含中子数为0.4NA | |
| B. | 在含有4molSi-O键的石英晶体中,氧原子数目为2 NA | |
| C. | 7.8克过氧化钠中,所含阴、阳离子总数为0.4NA | |
| D. | 28克N60单质中(如图),含的N-N键(σ键)个数为3 NA |
8.某溶液中所含离子的浓度如下表,则Mn+及a值可能分别为( )
| 离子 | NO3- | SO42- | H+ | Al3+ | Mn+ |
| 浓度(mol•L-1) | 3 | 4 | 2 | 2 | a |
| A. | Ag+、1.5 | B. | Mg2+、1.5 | C. | Ba2+、1.5 | D. | Fe3+、0.5 |
5.化学与生产、生活密切相关.下列说法不正确的是( )
| A. | 煤的干馏、石油的裂解都是化学变化 | |
| B. | 用CO2合成聚碳酸酯等可降解塑料,减少白色污染 | |
| C. | 光化学烟雾、硝酸型酸雨的形成都与氮氧化合物有关 | |
| D. | 人造纤维、合成纤维和光导纤维都属于有机高分子化合物 |
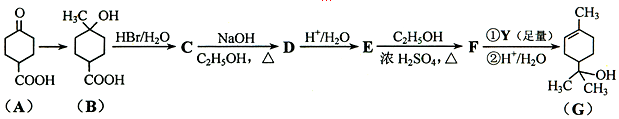
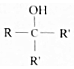
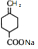 .
.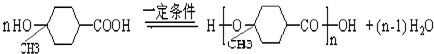 ;写出同时满足下列条件的B的链状同分异构体的结构简式
;写出同时满足下列条件的B的链状同分异构体的结构简式 .
.