题目内容
FeCl3溶液、Fe(OH)3胶体共同具备的性质是( )
| A、都呈透明的红褐色 |
| B、分散质颗粒直径相同 |
| C、都比较稳定,密封保存一段时间都不会产生沉淀 |
| D、都能产生丁达尔现象 |
考点:胶体的重要性质,分散系、胶体与溶液的概念及关系
专题:溶液和胶体专题
分析:A.根据FeCl3溶液与Fe(OH)3胶体的颜色分析解答;
B.溶液中溶质粒子小胶体粒子直径较大;
C.胶体具有介稳性,溶液具有稳定性;
D.只有胶体具有丁达尔效应,溶液不具备;
B.溶液中溶质粒子小胶体粒子直径较大;
C.胶体具有介稳性,溶液具有稳定性;
D.只有胶体具有丁达尔效应,溶液不具备;
解答:
解:A.因FeCl3溶液与Fe(OH)3胶体的颜色分别为棕黄色、红褐色,故A错误;
B.Fe(OH)3胶体的分散质颗粒直径在1-100nm之间,FeCl3溶液的分散质颗粒直径小于1nm,分散质颗粒直径不相同,故B错误;
C.胶体具有介稳性,放置不会产生沉淀,溶液是稳定的,故C正确;
D.只有胶体具有丁达尔效应,所以Fe(OH)3胶体具有丁达尔效应,而FeCl3溶液不具备,故D错误;
故选C.
B.Fe(OH)3胶体的分散质颗粒直径在1-100nm之间,FeCl3溶液的分散质颗粒直径小于1nm,分散质颗粒直径不相同,故B错误;
C.胶体具有介稳性,放置不会产生沉淀,溶液是稳定的,故C正确;
D.只有胶体具有丁达尔效应,所以Fe(OH)3胶体具有丁达尔效应,而FeCl3溶液不具备,故D错误;
故选C.
点评:本题考查了胶体的性质以及胶体和溶液的区别,题目难度不大,掌握胶体的性质是解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
不影响H2O的电离平衡的粒子是( )
A、 | ||
B、
| ||
C、 | ||
D、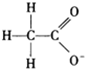 - - |
下列条件的变化,是因为降低反应所需的能量而增加单位体积内的反应物活化分子百分数致使反应速率加快的是( )
| A、增大浓度 | B、增大压强 |
| C、升高温度 | D、使用催化剂 |
用NA表示阿伏伽德罗常数,下列说法正确的是( )
| A、反应KClO3+6HCl=KCl+3Cl2↑+3H2O中,每生成1molCl2转移的电子为2NA |
| B、1molC8H18分子中含有的共用电子对数为26NA |
| C、在0℃,101kPa,1molSO3中含有NA个硫原子 |
| D、0.5L0.1mol/LNH4Cl溶液中含NH4+离子的数目为0.05NA |
25℃时,某稀溶液中由水电离产生的c(H+)为1×10-10,下列说法正确的是( )
| A、该溶液的pH不可能是7 |
| B、该溶液不可能存在 |
| C、该溶液的pH一定是10 |
| D、该溶液的pH一定是4 |