题目内容
在一定温度和压强下,2体积X2气体与3体积Y2气体恰好完全反应,生成2体积气体化合物Z,则Z的化学式可能是( )
| A、X2Y3 |
| B、XY |
| C、X2Y |
| D、XY3 |
考点:阿伏加德罗定律及推论
专题:
分析:一定温度和压强下,气体的体积之比等于物质的量之比,也等于化学计量数之比,然后利用质量守恒定律可得出Z的化学式.
解答:
解:一定温度和压强下,气体的体积之比等于物质的量之比,也等于化学计量数之比,
由2体积X2气体与3体积Y2气体恰好完全反应,生成2体积气体化合物Z,
反应方程式为:2X2+3Y2═2Z,
根据质量守恒定律可知,反应前后的原子个数相等,
所以Z的化学式为:X2Y3,
故选A.
由2体积X2气体与3体积Y2气体恰好完全反应,生成2体积气体化合物Z,
反应方程式为:2X2+3Y2═2Z,
根据质量守恒定律可知,反应前后的原子个数相等,
所以Z的化学式为:X2Y3,
故选A.
点评:本题考查阿伏伽德罗定律及其推论,题目难度中等,明确体积与化学计量数的关系及质量守恒定律是解答本题的关键,注意明确阿伏伽德罗定律及其推论的内容.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
某同学利用苹果可以制作水果原电池,如图所示.下列说法正确的是( )


| A、电流计指针偏转时,说明发生了氧化还原反应 |
| B、苹果汁中无电解质 |
| C、两个电极的材料可以相同 |
| D、水果电池工作时氧化反应和还原反应在同一处进行 |
已知:Fe(s)+
O2(g)═FeO(s)△H1=-272kJ/mol,2Al(s)+
O2(g)═Al2O3(s)△H2=-1 675kJ/mol,则2Al(s)+3FeO(s)═Al2O3(s)+3Fe(s)的△H是( )
| 1 |
| 2 |
| 3 |
| 2 |
| A、859 kJ/mol |
| B、-859 kJ/mol |
| C、-1403 kJ/mol |
| D、-2491 kJ/mol |
将28克铁粉溶于500mL的某稀硝酸溶液中,二者刚好完全反应,已知还原产物只有NO,且反应后的溶液比反应前增加了16克,则原硝酸浓度是( )mol/L.
| A、6.4 | B、4.8 |
| C、3.2 | D、2.4 |
阿伏加德罗常数约为6.02×1023mol-1,下列叙述中正确的是( )
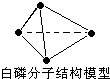

| A、31g 白磷分子(P4)中含有P-P键个数为1.5×6.02×1023 |
| B、48gO2和48gO3所含分子数为3×6.02×1023 |
| C、1.0L 1mol/L氨水中,NH3?H2O的分子数为6.02×1023 |
| D、20g 重水(D2O)中含有的中子数为8×6.02×1023 |
下列关于氢氧化铁胶体的叙述,正确的是( )
| A、往氢氧化铁胶体中逐滴加入稀盐酸先出现沉淀后沉淀溶解 |
| B、在含2 mol的氢氧化铁的胶体中含有氢氧化铁胶粒数为2NA |
| C、滤纸可将氢氧化铁胶体中的分散质与分散剂分离 |
| D、氢氧化铁胶体带正电荷 |
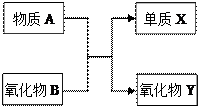 A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示,试写出符合下列条件的化学方程式:
A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如图所示,试写出符合下列条件的化学方程式: