题目内容
下列叙述错误的是( )
| A、铝热反应中可得到铁,但工业上不用该反应来大量生产铁 |
| B、可用蘸浓盐酸的棉棒检验输送氨气的管道是否漏气 |
| C、明矾和漂白粉常用于自来水的净化和杀菌消毒,两者原理相同 |
| D、生成盐和水的反应不一定是中和反应 |
考点:氨的化学性质,胶体的重要性质,氧化还原反应,铝的化学性质
专题:
分析:A.工业炼铁的原理是在高温条件下用一氧化碳还原铁的氧化物,通常是还原氧化铁;
B.浓盐酸和NH3反应生成固体NH4Cl;
C.胶体具有吸附性而净水,漂白粉有氧化性而杀菌消毒;
D.生成盐和水的反应可能是中和反应也可能不是中和反应.
B.浓盐酸和NH3反应生成固体NH4Cl;
C.胶体具有吸附性而净水,漂白粉有氧化性而杀菌消毒;
D.生成盐和水的反应可能是中和反应也可能不是中和反应.
解答:
解:A.工业炼铁的原理是用一氧化碳还原铁的氧化物,铝热反应中可得到铁,可用于焊接铁轨,但造价太高,所以不能大量生产铁,故A正确;
B.浓盐酸和NH3反应生成固体NH4Cl,产生白烟,故B正确;
C.明矾中的铝离子易水解生成氢氧化铝胶体,胶体具有吸附性而净水,漂白粉中次氯酸钙具有强氧化性,能使蛋白质变性而杀菌消毒,所以二者原理不同,故C错误;
D.生成盐和水的反应可能是中和反应也可能不是中和反应,如Al2O3+6HCl=2AlCl3+3H2O,故D正确;
故选C.
B.浓盐酸和NH3反应生成固体NH4Cl,产生白烟,故B正确;
C.明矾中的铝离子易水解生成氢氧化铝胶体,胶体具有吸附性而净水,漂白粉中次氯酸钙具有强氧化性,能使蛋白质变性而杀菌消毒,所以二者原理不同,故C错误;
D.生成盐和水的反应可能是中和反应也可能不是中和反应,如Al2O3+6HCl=2AlCl3+3H2O,故D正确;
故选C.
点评:本题考查较综合,涉及中和反应概念、氨气的检验、金属的冶炼、水的净化等知识点,侧重考查学生分析问题、解答问题能力,明确物质的性质即可解答,易错选项是C,注意二者区别.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列说法不正确的是( )
| A、氟氯烃的肆意排放会加速臭氧层的破坏,使大气层中的紫外线增强 |
| B、除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤后分液、干燥、蒸馏即可 |
| C、淀粉、蛋白质、油脂均是天然高分子化合物 |
| D、不慎将苯酚沾到皮肤上应立即用酒精清洗 |
下列有关说法体现了化学与生产、生活、社会的密切关系. 其中不正确的是( )
| A、绚丽缤纷的烟花中添加了含钾、钠、钙、铜等金属元素的化合物 |
| B、为防止中秋月饼等富脂食品氧化变质,常在包装袋中放入生石灰 |
| C、停车场安装催化光反应设施,可使汽车尾气中的CO和NOX反应生成无毒气体 |
| D、氮化硅陶瓷、氧化铝陶瓷、光导纤维等属于新型无机非金属材料 |
为更好地表示溶液的酸碱性,科学家提出了酸度(AG)的概念:AG=1g
,则下列叙述不正确的是( )
| c(H+) |
| c(OH-) |
| A、中性溶液的AG=0 |
| B、碱性溶液的AG>0 |
| C、AG越小碱性越强,酸性越弱 |
| D、常温下0.1mol?L-1氢氧化钠溶液的AG=-12 |
下列叙述正确的是( )
| A、SiO2和A12O3都既能与酸反应,又能与碱反应 |
| B、硫化钠溶于水中发生反应的离子方程式为S2-+2H2O?H2S+2OH- |
| C、3.2 g Cu与5.5 mL l8.4 mol?L -1的浓H2SO4充分反应,转移的电子数为6.02×1022 |
| D、由水电离的c(H+)=1×10 -13mol?L -1的溶液中Cl-、HCO3-、NO3-、NH4+能大量共存 |
在下列条件下,能大量共存的微粒组是( )

| A、c(H+)=1×10-14mol/L的溶液:K+、Na+、AlO2-、S2O32- |
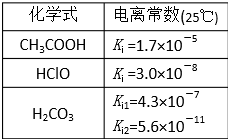
| B、上表提供的数据下:HClO、HCO3-、ClO-、CO32- |
| C、能与Al反应生成H2的溶液:NH4+、Ca2+、NO3-、I- |
| D、中性的溶液中:CO32-、Na+、SO42-、AlO2- |
下列各组物质的颜色变化,可用勒夏特列原理解释的是( )
| A、新制的氯水在光照条件下颜色变浅 |
| B、H2、I2、HI平衡混合气加压后颜色变深 |
| C、氯化铁溶液加铁粉振荡后颜色变浅 |
| D、加入催化剂有利于氨的催化氧化 |