题目内容
【题目】在不同温度下,水溶液中c(H+)与c(OH﹣)有如图所示关系,下列有关说法正确的是( ) 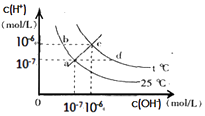
A.c点对应的溶液中大量存在的离子可能为:Na+、H+、Cl﹣、NO3﹣
B.将25℃时的KCl溶液加热到t℃,则该溶液中的c(OH﹣)由a点变化到b点
C.t℃<25℃
D.ac线上的任意一点溶液均有c(H+)=c(OH﹣)
【答案】D
【解析】解:A.c点溶液中c(H+)=c(OH﹣),溶液呈中性,如果溶液中存在Na+、H+、Cl﹣、NO3﹣ , 则该溶液呈酸性,不符合,故A错误;
B.KCl溶液呈中性,升高温度增大水的电离,但溶液仍然呈中性,a点溶液呈中性,但b点c(H+)>c(OH﹣),故B错误;
C.水的电离是吸热反应,升高温度促进水电离,水的离子积常数增大,根据图知,a点离子积常数小于c,所以t℃>25℃,故C错误;
D.ac线上任一点都呈中性,所以都存在c(H+)=c(OH﹣),故D正确;
故选D.
【考点精析】关于本题考查的离子积常数,需要了解水的离子积Kw=c(H+)·c(OH–)=10–14(25℃)①Kw只与温度有关,温度升高,Kw增大;如:100℃ Kw=10–12②Kw适用于纯水或稀酸、稀碱、稀盐水溶液中才能得出正确答案.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目