题目内容
下列各组物质的熔沸点高低只与范德华力有关的是( )
| A、HI HBr HCl HF |
| B、Li Na K Rb |
| C、LiCl HCl HBr RbCl |
| D、F2 Cl2 Br2 I2 |
考点:分子间作用力对物质的状态等方面的影响
专题:化学键与晶体结构
分析:不能形成氢键的分子晶体的熔沸点只与范德华力有关.
解答:
解:A、HF分子间能形成氢键,因HF的熔沸点还与氢键有关,故A不选;
B、Li Na K Rb的熔沸点与金属键有关,故B不选;
C、LiCl,RbCl的熔沸点与离子键有关,故C不选;
D、都是分子晶体,熔化或者蒸发的时候只克服范德华力,所以熔沸点只与范德华力有关;
故选D.
B、Li Na K Rb的熔沸点与金属键有关,故B不选;
C、LiCl,RbCl的熔沸点与离子键有关,故C不选;
D、都是分子晶体,熔化或者蒸发的时候只克服范德华力,所以熔沸点只与范德华力有关;
故选D.
点评:本题考查了分子间作用力对物质的状态的影响,题目难度不大,注意不能形成氢键的分子晶体的熔沸点只与范德华力有关,正确判断晶体类型是解题的关键.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
摩尔质量为M g/mol的某物质在20℃时的溶解度为Sg/100g水,其20℃的饱和溶液的密度为d g/mL,其物质的量浓度为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列说法正确的是( )
| A、铁溶于稀硝酸,溶液变黄:3Fe+8H++2NO3-═3Fe2++2NO↑+4H2O |
| B、向氢氧化亚铁中加入足量的稀硝酸:Fe(OH)2+2H+═Fe2++2H2O |
| C、向含有少量FeCl3的MgCl2溶液中加入足量Mg(OH)2粉末,搅拌一段时间后过滤,目的是除去MgCl2溶液中少量的FeCl3 |
| D、用FeCl3溶液腐蚀铜线路板:Cu+Fe3+═Cu2++Fe2+ |
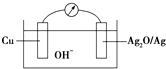 普通水泥在固化过程中自由水分子减少并产生Ca(OH)2,溶液呈碱性.根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间. 此方法的原理如图所示,反应的总方程式为:2Cu+Ag2O═Cu2O+2Ag,下列有关说法正确的是( )
普通水泥在固化过程中自由水分子减少并产生Ca(OH)2,溶液呈碱性.根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间. 此方法的原理如图所示,反应的总方程式为:2Cu+Ag2O═Cu2O+2Ag,下列有关说法正确的是( )| A、普通水泥的主要成分是2CaO?SiO2,3CaO?SiO2和3CaO?Al2O3 |
| B、测量原理示意图中,Ag2O为负极 |
| C、正极的电极反应为:2Cu+2OH--2e-═Cu2O+H2O |
| D、电池工作时,OH-向正极移动 |
醇类化合物在香料中占有重要的地位,下面所列的是一些天然的或合成的醇类香料:
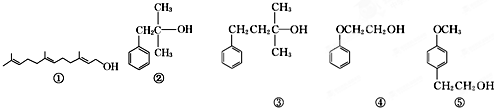
下列说法中正确的是( )

下列说法中正确的是( )
| A、可用酸性KMnO4溶液检验①中是否含有碳碳双键 |
| B、②和③互为同系物,均能催化氧化生成醛 |
| C、④和⑤互为同系物,可用核磁共振氢谱检验 |
| D、等物质的量的上述5种有机物与足量的金属钠反应,消耗钠的量相同 |
下列物质中不能通过置换反应生成的是( )
| A、Al2O3 |
| B、F2 |
| C、Fe3O4 |
| D、C |
 反应N2(g)+3H2(g)?2NH3(g);△H<0在等容条件下进行.改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示.下列说法不正确的是( )
反应N2(g)+3H2(g)?2NH3(g);△H<0在等容条件下进行.改变其他反应条件,在Ⅰ、Ⅱ、Ⅲ阶段体系中各物质浓度随时间变化的曲线如图所示.下列说法不正确的是( )| A、第Ⅱ阶段反应温度(T2)和第Ⅲ阶段反应温度(T3):T2<T3 |
| B、Ⅰ、Ⅱ、Ⅲ三个阶段H2的转化率:αⅠ(H2)>αⅡ(H2)>αⅢ(H2) |
| C、Ⅰ、Ⅱ、Ⅲ三个阶段平均反应速率:vⅠ(N2)>vⅡ(N2)>vⅢ(N2) |
| D、第Ⅱ阶段采取的措施是将NH3从第Ⅰ阶段平衡混合物中分离出去 |
下列物质中与苯互为同分异构体的是( )
| A、CH3(CH═CH)2CH3 |
B、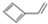 |
C、 |
D、 |