题目内容
7.下列关于电解质的电离平衡状态的叙述中,正确的是( )| A. | 弱电解质的电离达到平衡状态后,电离就停止了 | |
| B. | 弱电解质的电离达到平衡状态后,分子的消耗速率和离子的生成速率相等 | |
| C. | 弱电解质的电离达到平衡状态后,分子和离子的浓度相等 | |
| D. | 弱电解质的电离达到平衡状态后,外界条件改变,电离平衡可能要发生移动 |
分析 弱电解质电离达到平衡状态时,电解质的电离速率与离子结合生成电解质的速率相等,达到动态平衡状态,反应体系中各微粒的物质的量、物质的量浓度、百分含量以及由此引起的一系列物理量不变,据此分析解答.
解答 解:A.电解质电离达到平衡状态后,电解质的电离速率与离子结合生成电解质的速率相等,达到动态平衡状态,故A错误;
B.无论是否达到平衡状态,都存在分子的消耗速率和离子的生成速率相等,故B错误;
C.弱电解质的电离达到平衡状态后,分子和离子的浓度都不变,但不一定相等,故C错误;
D.弱电解质的电离达到平衡状态后,正逆反应速率相等,反应为动态平衡状态,但外界条件改变,电离平衡可能被打破,所以可能要发生移动,从新达到新的平衡状态,故D正确;
故选D.
点评 本题考查弱电解质的电离,为高频考点,明确弱电解质电离特点及电离平衡状态特征是解本题关键,侧重考查学生分析判断能力,题目难度不大.

练习册系列答案
相关题目
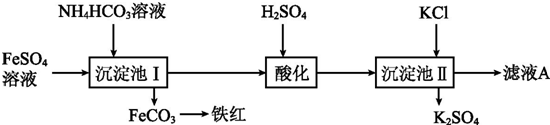
17.为处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏.化学家研究在催化条件下,通过下列反应,使CCl4转化为重要的化工原料氯仿(CHCl3).CCl4+H2?CHCl3+HCl△H<0 已知CCl4的沸点为77℃,CHCl3的沸点为61.2℃.
(1)在密闭器中,该反应达到平衡后,测得如表数据.
①实验1中,10h后达到平衡,H2的平均反应速率为0.05mol•L-1•h-1.在此实验的平衡体系中,再加入0.5molCCl4和0.5molHCl,平衡将不移动(“向左”、“向右”、“不”或“无法确定”).
②实验2中,X的值B(填序号).
A.等于50% B.大于50% C.小于50% D.无法确定
③实验3中的Y值为1.2.
(2)为从平衡体系CCl4+H2?CHCl3+HCl中分离得到CHCl3,请你结合题给信息设计合理的方案,用简要的文字表示:先把平衡体系中的混合物降温到61.2℃以下得到CCl4和CHCl3液态混合物,再分馏得到CHCl3.
(1)在密闭器中,该反应达到平衡后,测得如表数据.
| 实验序号 | 温度(℃) | 初始CCl4浓度(mol•L-1) | 初始H2浓度(mol•L-1) | CCl4的平衡转化率 |
| 1 | 110 | 1 | 1 | 50% |
| 2 | 100 | 1 | 1 | X |
| 3 | 110 | 0.8 | Y | 60% |
②实验2中,X的值B(填序号).
A.等于50% B.大于50% C.小于50% D.无法确定
③实验3中的Y值为1.2.
(2)为从平衡体系CCl4+H2?CHCl3+HCl中分离得到CHCl3,请你结合题给信息设计合理的方案,用简要的文字表示:先把平衡体系中的混合物降温到61.2℃以下得到CCl4和CHCl3液态混合物,再分馏得到CHCl3.
18.下列说法中不正确的是( )
| A. | 乙烯分子中C═C双键中有一个键容易断裂 | |
| B. | 乙烯分子中6个原子共平面 | |
| C. | 不能用酸性高锰酸钾溶液除去乙烷中混有的乙烯 | |
| D. | 乙烷和乙烯都能使溴水褪色 |
2.在恒温条件下,有甲、乙两容器,甲容器为体积不变的密闭容器,乙容器为一个带有理想活塞(即无质量、无摩擦力的刚性活塞)的体积可变的密闭容器,两容器起始状态完全相同,都充有C气体,若发生可逆反应C(g)?A(g)+B(g),经一段时间后,甲、乙两容器反应都达到平衡.下列说法中正确的是( )
| A. | 平均反应速度:乙>甲 | B. | 平衡时nc(甲)>nc(乙) | ||
| C. | 平衡时C的转化率:甲>乙 | D. | 平衡时A的物质的量甲>乙 |
12.下列说法中,不正确的是( )
| A. | 1 mol乙烯与Cl2完全加成,然后与Cl2发生取代反应,共消耗氯气5mol | |
| B. | 溴水遇到乙醛溶液出现褪色现象,是因为它们发生了氧化反应 | |
| C. | 乙烯与苯都能使溴水褪色,但褪色原理不同 | |
| D. | 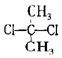 与 与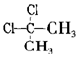 互为同分异构体 互为同分异构体 |
19.当反应:N2(g)+3H2(g)?2NH3(g)△H1<0达到平衡状态时,下列选项中一定能使该反应朝正反应方向移动的是( )
| A. | 升高温度 | B. | 加入催化剂 | C. | .增大H2(g)的浓度 | D. | 增大NH3(g)的浓度 |
16.以下说法正确的是( )
| A. | 还原剂中必定有元素化合价升高被氧化 | |
| B. | 通电后,氢氧化铁胶体向阴极运动 | |
| C. | 物质所含元素化合价升高的反应叫还原反应 | |
| D. | 胶体与其他分散系的本质区别是可以发生丁达尔效应 |