题目内容
如图所示为某研究性学习小组探究金属腐蚀条件的实验装置图,试分析实验并回答下列问题:

(1)起始时若甲、乙、丙三套装置的导管中液面高度相同,则过一段时间后导管中液面最高的是 (填装置代号).
(2)通过甲、乙装置的对比实验说明,钢铁中碳的含量越 (填“高”或“低”)越容易被腐蚀.
(3)乙装置中发生电化学腐蚀时正极的电极反应式为 .
(4)为防止铁的锈蚀,工业上普遍采用的方法是 (写出一点即可).

(1)起始时若甲、乙、丙三套装置的导管中液面高度相同,则过一段时间后导管中液面最高的是
(2)通过甲、乙装置的对比实验说明,钢铁中碳的含量越
(3)乙装置中发生电化学腐蚀时正极的电极反应式为
(4)为防止铁的锈蚀,工业上普遍采用的方法是
考点:金属的电化学腐蚀与防护
专题:电化学专题
分析:(1)乙形成了原电池,丙浸没在非电解质溶液中,故腐蚀速率乙>甲>丙;
(2)含碳量越高,容易形成原电池,所以越易腐蚀;
(3)乙发生吸氧腐蚀,发生电化学腐蚀时正极氧气得到电子生成氢氧根离子;
(4)根据金属防护的方法知识来回答.
(2)含碳量越高,容易形成原电池,所以越易腐蚀;
(3)乙发生吸氧腐蚀,发生电化学腐蚀时正极氧气得到电子生成氢氧根离子;
(4)根据金属防护的方法知识来回答.
解答:
解:(1)甲为铁粉在氯化钠溶液中的腐蚀,乙为铁粉与碳形成原电池的腐蚀,而丙的腐蚀没有电解质溶液,所以腐蚀的速率大小为:乙>甲>丙,故过一段时间后液面最高的是乙,故答案为:乙;
(2)甲中为铁粉,乙为铁粉与碳粉的混合物,甲的腐蚀速率小于乙的,通过甲、乙装置的对比说明钢铁中碳的含量越高,钢铁越易腐蚀,
故答案为:高;
(3)乙装置中发生电化学腐蚀时,分解铁失去电子,正极氧气得到电子生成氢氧根离子,正极的电极反应式为:O2+4e-+2H2O═4OH-,
故答案为:O2+4e-+2H2O═4OH-;
(4)金属的防护措施有牺牲阳极的阴极保护法、外加电流的阴极保护法,另外还有电镀、喷镀、喷油漆等方法使金属与空气、水等物质隔离,以防止金属腐蚀,
故答案为:牺牲阳极的阴极保护法或者外加电流的阴极保护法.
(2)甲中为铁粉,乙为铁粉与碳粉的混合物,甲的腐蚀速率小于乙的,通过甲、乙装置的对比说明钢铁中碳的含量越高,钢铁越易腐蚀,
故答案为:高;
(3)乙装置中发生电化学腐蚀时,分解铁失去电子,正极氧气得到电子生成氢氧根离子,正极的电极反应式为:O2+4e-+2H2O═4OH-,
故答案为:O2+4e-+2H2O═4OH-;
(4)金属的防护措施有牺牲阳极的阴极保护法、外加电流的阴极保护法,另外还有电镀、喷镀、喷油漆等方法使金属与空气、水等物质隔离,以防止金属腐蚀,
故答案为:牺牲阳极的阴极保护法或者外加电流的阴极保护法.
点评:本题考查了金属的电化学腐蚀、原电池工作原理,题目难度中等,注意掌握原电池工作原理,明确金属腐蚀快慢比较方法:(1)电解原理引起的阳极腐蚀>原电池原理引起的负极腐蚀>化学腐蚀>有防护措施的腐蚀;(2)对同一种金属,腐蚀的快慢:强电解质溶液>弱电解质溶液>非电解质溶液;活泼性不同的两种金属,活泼性差别越大,腐蚀越快;(3)对同一种电解质溶液,电解质溶液浓度越大,腐蚀越快;(4)由于金属表面一般不会遇到酸性较强的溶液,故吸氧腐蚀是金属腐蚀的主要形式;另外,只有在金属活动性顺序表中位于氢前面的金属才可能发生析氢腐蚀,而位于氢之后的金属腐蚀只能是吸氧腐蚀.

练习册系列答案
相关题目
寿山石的主要成分为叶腊石,其组成为Al2O3?4SiO2?H2O,可以表示为Al2Si4Ox(OH)y.其中x、y的数值分别是( )
| A、10、2 | B、6、4 |
| C、8、2 | D、2、8 |
用括号中的试剂和操作方法除去各组中的杂质,不正确的是( )
| A、苯中的甲苯(溴水分液) |
| B、乙醇中的水(新制CaO蒸馏) |
| C、乙醛中的乙酸(NaOH蒸馏) |
| D、乙酸乙酯中的乙酸(饱和Na2CO3溶液分液) |
利用如图装置,其中不能实现铁的电化学防护的一组是( )
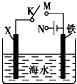

| A、X为锌,开关K置于M处 |
| B、X为锌,开关K置于N处 |
| C、X为铜,开关K置于M处 |
| D、X为碳棒,开关K置于N处 |
下列说法正确的是( )
| A、向CCl4中加入硝酸银溶液,可以鉴定其中的氯原子 |
| B、淀粉和纤维素互为同分异构体,因为二者的通式相同,都是(C6H10 O5)n |
| C、向米汤中加入加碘食盐,观察是否有颜色的变化--检验加碘食盐中是否含碘酸钾 |
| D、由油脂得到甘油,淀粉得到葡萄糖,均发生了水解反应 |
下列物质中,能导电且为电解质的是( )
| A、熔融态KNO3 |
| B、固体NaCl |
| C、Cu |
| D、NaOH溶液 |
下列说法正确的是( )
| A、分别向Na2CO3和NaHCO3溶液中滴加澄清石灰水,都能生成白色沉淀 |
| B、分别向FeCl2、FeCl3溶液中滴入NaOH溶液,溶液中都立即出现红褐色沉淀 |
| C、等质量的Al分别与过量的NaOH、HCl溶液反应,NaOH溶液中放出的多 |
| D、向等物质的量的Na2CO3和NaHCO3溶液中分别滴入足量的稀HC1,前者生成的CO2多 |