题目内容
氨在国民经济中占有重要地位。
(1)NH3的电子式为
(2)实验室中制取氨气的化学方程式为 ,
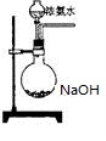
(3)欲快速制取氨气,可将浓氨水滴入固体氢氧化钠中,其装置如下图,请结合化学用语 从化学平衡的角度解释:
(4)将SO2气体通入氯化钡溶液,未见有沉淀生成,继续通入NH3,则出现白色沉淀,请写出反应的离子方程式 ;若将SO2气体通入酸化的硝酸钡溶液,也产生白色沉淀,用离子方程式加以说明
(5)氨和肼(N2H4)是氮的两种常见化合物,在科学技术和生产中有重要的应用。
肼——空气燃料电池是一种碱性电池,该电池放电时,负极的反应式 。
(6)氮氧化物的排放会对空气造成污染,利用氧化法除去烟气中的氮氧化物。
首先向氮氧化物中补充氧气,然后将混合气体通入石灰乳中,使之转化为硝酸钙。
已知某氮氧化物由NO和NO2组成,且n(NO):n(NO2)=1:3.
写出氧化吸收法除去氮氧化物的化学方程式______________ _____
(1)
(2)Ca(OH)2+2NH4Cl CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
(3)NH3+H2O NH3?H2O
NH3?H2O NH4++OH?,NaOH溶于水发生电离,使c(OH?)增大,平衡向生成NH3的方向移动,NH3逸出。
NH4++OH?,NaOH溶于水发生电离,使c(OH?)增大,平衡向生成NH3的方向移动,NH3逸出。
(4)2NH3+SO2+H2O+Ba2+=BaSO4↓+2NH4+(1分)(答案合理即给分)
3SO2+2H2O+2NO3?+3Ba2+=3BaSO4↓+2NO↑+4H+(1分)(答案合理即给分)
(5)N2H4+4OH--4e-=4H2O+N2↑(2分)
(6)3O2+2NO+6NO2+4Ca(OH)2=4Ca(NO3)2+4H2O
【解析】
试题分析:(1)NH3分子中N与3个H原子分别形成一对共用电子,电子式为: 。
。
(2)实验室用Ca(OH)2与NH4Cl加热制取NH3,化学方程式为:Ca(OH)2+2NH4Cl CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。
(3)浓氨水中存在下列平衡:NH3+H2O NH3?H2O
NH3?H2O NH4++OH?,NaOH为强碱,溶于水发生电离,使c(OH?)增大,平衡向生成NH3的方向移动,NH3逸出。
NH4++OH?,NaOH为强碱,溶于水发生电离,使c(OH?)增大,平衡向生成NH3的方向移动,NH3逸出。
(4)继续通入NH3,SO2与NH3反应生成(NH4)2SO3,SO32?与Ba2+结合生成BaSO4,离子方程式为:2NH3+SO2+H2O+Ba2+=BaSO4↓+2NH4+;将SO2气体通入酸化的硝酸钡溶液,SO2被氧化为SO42?,结合Ba2+生成BaSO4,离子方程式为:3SO2+2H2O+2NO3?+3Ba2+=3BaSO4↓+2NO↑+4H+
(5)肼-氧气碱性燃料电池中,负极上燃料肼失电子和氢氧根离子反应生成水和氮气,电极反应式为N2H4+4OH--4e-=4H2O+N2↑
(6)设一氧化氮为1mol,则二氧化氮为3mol,1mol一氧化氮转化成硝酸根离子失去3mol电子,3mol二氧化氮转化成硝酸失去3mol电子,总共失去6mol电子,需要消耗氧气的物质的量为6mol÷4=1.5mol,由于化学方程式中不能出现分数,则消耗氧气的计量数为3,一氧化氮和二氧化氮的计量数分别为2、6,该反应的化学方程式为:3O2+2NO+6NO2+4Ca(OH)2=4Ca(NO3)2+4H2O
考点:本题考查电子式、NH3的实验室制法、平衡移动、原电池原理、方程式的书写。

向四支试管中分别加入少量不同的无色溶液进行如下操作,结论正确的是( )
| 操作 | 现象 | 结论 |
A | 滴加BaCl2溶液 | 生成白色沉淀 | 原溶液中有SO42- |
B | 滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有Na+,无K+ |
D | 滴加稀NaOH溶液,将湿润红色石蕊试纸置于试管口 | 试纸不变蓝 | 原溶液中无NH4+ |
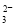 ===HCO
===HCO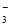 ③CO2+H2O+ClO-===HClO+HCO
③CO2+H2O+ClO-===HClO+HCO