题目内容
硅及其化合物的应用范围很广.下列说法正确的是( )
| A、硅是人类将太阳能转换为电能的常用材料 | B、粗硅制备单晶硅不涉及氧化还原反应 | C、石英玻璃和餐桌上的瓷盘都是硅酸盐制品 | D、盐酸可以与硅反应,故采用盐酸为抛光液抛光单晶硅 |
分析:A.太阳能电池的材料是硅单质;
B.凡是有化合价变化的反应为氧化还原反应;
C.石英玻璃的成分是二氧化硅;
D.硅单质只能与氢氟酸反应.
B.凡是有化合价变化的反应为氧化还原反应;
C.石英玻璃的成分是二氧化硅;
D.硅单质只能与氢氟酸反应.
解答:解:A.硅单质是太阳能电池的材料,故A正确;
B.由粗硅制备单晶硅涉及氧化还原反应,方程式为SiO2+2C
Si+2CO↑,故B错误;
C.石英玻璃的成分是二氧化硅,不是硅酸盐,故C错误;
D.盐酸与硅不反应,故D错误.
故选A.
B.由粗硅制备单晶硅涉及氧化还原反应,方程式为SiO2+2C
| ||
C.石英玻璃的成分是二氧化硅,不是硅酸盐,故C错误;
D.盐酸与硅不反应,故D错误.
故选A.
点评:本题考查硅及其化合物的性质和用途,难度不大,注意硅单质只能与氢氟酸反应,与一般的酸不反应.

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目
铁铜单质及其化合物的应用范围很广。现有含氯化亚铁杂质的氯化铜晶体(CuCl2·2H2O),为制取纯净的CuCl2·2H2O,首先将其制成水溶液,然后按照如图步骤进行提纯:
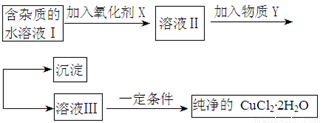
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH见下表:
|
|
Fe3+ |
Fe2+ |
Cu2+ |
|
氢氧化物开始沉淀时的pH |
1.9 |
7.0 |
4.7 |
|
氢氧化物沉淀完全时的pH |
3.2 |
9.0 |
6.7 |
请回答下列问题:
(1)加入氧化剂的目的是
(2)下列最适合作氧化剂X的是
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(3)加入的物质Y是
(4)如果不用物质Y而直接用可溶性碱溶液能不能达到目的? (填“能”或者“不能”)。若不能,试解释原因 (若填“能”,此空不用回答)
(5)最后能不能直接蒸发得到CuCl2·2H2O? (填“能”或者“不能”)。若不能,应该如何操作才能得到CuCl2·2H2O (若填“能”,此空不用回答)
(6)若向溶液Ⅱ中加入碳酸钙,产生的现象是
(7)若向溶液Ⅱ中加入镁粉,产生的气体是 ,试解释原因
(8)FeCl3溶液具有净水作用的原因是