��Ŀ����
1�����º����£���2molA�����2molB����ͨ�����Ϊ2L���ܱ������з������·�Ӧ��2A��g��+2B��g��?xC��g��+2D��g����2minʱ��Ӧ�ﵽƽ��״̬����ʱʣ��1.2mol B�������C��Ũ��Ϊ1.2mo1•L-1����1���ӿ�ʼ��Ӧ���ﵽƽ��״̬������C��ƽ����Ӧ����Ϊ0.6mol/��L��min����
��2��x=6��
��3��A��ת������B��ת����֮��Ϊ1��1��
��4�����������ݻ����䣬�����м���amolHe����÷�Ӧ������Ӧ����Ϊ���䣨�����С�����䡱����ƽ�⽫���ƶ���������ƶ����������ƶ������ƶ�������
���� 2minʱ��Ӧ�ﵽƽ��״̬����ʱʣ��1.2mol B�������C��Ũ��Ϊ1.2mo1•L-1��v��B��=$\frac{\frac{2mol-1.2mol}{2L}}{2min}$=0.2mol/��L��min����v��C��=$\frac{1.2mol/L}{2min}$=0.6mol/��L��min�����ɷ�Ӧ����֮�ȵ��ڻ�ѧ������֮�ȿ�֪��x=6����
2A��g��+2B��g��?6C��g��+2D��g��
��ʼ 2 2 0 0
ת�� 0.8 0.8 2.4 0.8
ƽ�� 1.2 1.2 2.4 0.8
�Դ˿ɼ���ת���ʣ�
��4�������ݻ����䣬�����м���amolHe����Ӧ��ϵ�и����ʵ�Ũ�Ȳ��䣮
��� �⣺2minʱ��Ӧ�ﵽƽ��״̬����ʱʣ��1.2mol B�������C��Ũ��Ϊ1.2mo1•L-1��v��B��=$\frac{\frac{2mol-1.2mol}{2L}}{2min}$=0.2mol/��L��min����v��C��=$\frac{1.2mol/L}{2min}$=0.6mol/��L��min�����ɷ�Ӧ����֮�ȵ��ڻ�ѧ������֮�ȿ�֪��x=6����
2A��g��+2B��g��?6C��g��+2D��g��
��ʼ 2 2 0 0
ת�� 0.8 0.8 2.4 0.8
ƽ�� 1.2 1.2 2.4 0.8
��1�������������֪���ӿ�ʼ��Ӧ���ﵽƽ��״̬������C��ƽ����Ӧ����Ϊ0.6mol/��L��min�����ʴ�Ϊ��0.6mol/��L��min����
��2��x=6���ʴ�Ϊ��6��
��3��A��ת������B��ת����֮��Ϊ$\frac{0.8}{2}$��$\frac{0.8}{2}$=1��1���ʴ�Ϊ��1��1��
��4�����������ݻ����䣬�����м���amolHe����Ӧ��ϵ�и����ʵ�Ũ�Ȳ��䣬��÷�Ӧ������Ӧ����Ϊ���䣬ƽ�⽫���ƶ����ʴ�Ϊ�����䣻���ƶ���
���� ���⿼�黯ѧƽ��ļ��㣬Ϊ��Ƶ���㣬���ջ�ѧƽ�����η���ת���ʼ����Ϊ���Ĺؼ������ط�������������Ŀ��飬ע�⻯ѧ���������жϣ���Ŀ�ѶȲ���

| A�� | ��Ȼֲ���ͳ�����һ���Һ̬��������ˮ��û�к㶨���۵㡢�е� | |
| B�� | ��ȩ������������Ƕ��������Ƶ�Cu��OH��2��Ӧ���ҷ�Ӧ���;�Ϊ������Ӧ | |
| C�� | ��ȩ������ϩ���Ҷ���������Ϊ�ϳɾۺ���ĵ��� | |
| D�� | ʯ�ʹ��ѻ�����ҪĿ����������͵������͵IJ�����������ʯ���ѽ����ҪĿ���ǵõ��������ϩ����ϩ����̬������ |
 ijʵ��С����0.50mol/L NaOH��Һ��0.50mol/L H2SO4��Һ�����к��ȵIJⶨ��
ijʵ��С����0.50mol/L NaOH��Һ��0.50mol/L H2SO4��Һ�����к��ȵIJⶨ��������0.50mol/L NaOH��Һ
��1����ʵ���д�ԼҪʹ��245mL NaOH��Һ����������Ҫ����NaOH����5.0g��
��2���ӱ�ͼ��ѡ�����NaOH��������Ҫ������������ţ�abe��
| ���� | ������ƽ�������룩 | С�ձ� | ����ǯ | ������ | ҩ�� | ��Ͳ |
| ���� |  |  |  |  |  |  |
| ��� | a | b | c | d | e | f |
��1��д��ϡ�����ϡ����������Һ��Ӧ��ʾ�к��ȵ��Ȼ�ѧ����ʽ���к�����ֵ57.3kJ/mol����$\frac{1}{2}$H2SO4��aq��+NaOH��aq���T$\frac{1}{2}$Na2SO4��aq��+H2O��l����H=-57.3kJ/mol
��2��ȡ50mL NaOH��Һ��30mL�������ʵ�飬ʵ���������±���
������д�±��еĿհף�
| ʵ����� �¶� | ��ʼ�¶�t1/�� | ��ֹ�¶�t2/�� | ƽ���¶Ȳ� ��t2-t1��/�� | ||
| H2SO4 | NaOH | ƽ��ֵ | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
������ʵ��������ֵ��57.3kJ/mol��ƫ�����ƫ���ԭ������ǣ�����ĸ��acd��
a��ʵ��װ�ñ��¡�����Ч����
b������ȡNaOH��Һ�����ʱ���Ӷ���
c���ֶ�ΰ�NaOH��Һ����ʢ��ϡ�����С�ձ���
d�����¶ȼƲⶨNaOH��Һ��ʼ�¶Ⱥ�ֱ�ӲⶨH2SO4��Һ���¶ȣ�
| A�� | ${\;}_{8}^{17}O$ԭ�Ӻ��ں���8������ | B�� | ${\;}_{8}^{17}O$ԭ�Ӻ��ں���8������ | ||
| C�� | ${\;}_{8}^{17}O$ԭ�Ӻ�����17������ | D�� | ${\;}_{8}^{17}O$ԭ�Ӻ��ں���17������ |
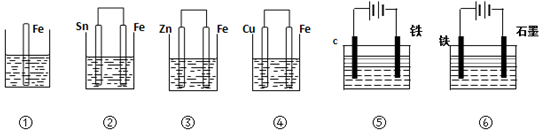
| A�� | �ܣ��ڣ��٣��ۣ��ݣ��� | B�� | �ޣ��ܣ��ڣ��٣��ۣ��� | C�� | �ܣ��ڣ��ݣ��ۣ��ޣ��� | D�� | �ޣ��ۣ��ڣ��ܣ��٣��� |
| A�� | Co2O3+6HCl=2CoCl2+Cl2��+3H2O�У��������ͻ�ԭ�����ʵ���֮��Ϊ1��6 | |
| B�� | 5KI+KIO3+3H2SO4=3I2+3K2SO4+3H2O�У���������ͻ�ԭ�������ʵ���֮��Ϊ5��1 | |
| C�� | 3S8+24KOH=8K2SO3+4K2S4+12H2O�У��������ͱ���ԭ��S8���ʵ���֮��Ϊ2��1 | |
| D�� | 3��NH4��2SO4=3SO2+N2+6H2O+4NH3�У���Ӧ�з���������Ӧ��δ����������Ӧ�ĵ�Ԫ�����ʵ���֮��Ϊ2��1 |
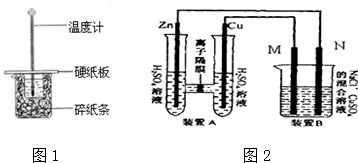
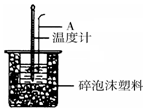 50mL 0.50mol/L�����50mL 0.55mol/L NaOH��Һ����ͼ��ʾ��װ�� �н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ��㷴Ӧ�ȣ�
50mL 0.50mol/L�����50mL 0.55mol/L NaOH��Һ����ͼ��ʾ��װ�� �н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ��㷴Ӧ�ȣ�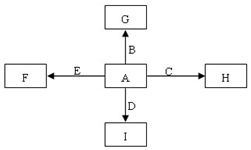 ͼ�У�A��B��C��D��E�ǵ��ʣ�G��H��I��F��B��C��D��E�ֱ��A�γɵĶ�Ԫ�������֪���ٷ�ӦC+G$\stackrel{����}{��}$B+H�ܷų��������ȣ��÷�Ӧ��Ӧ��������ĺ��ӣ�
ͼ�У�A��B��C��D��E�ǵ��ʣ�G��H��I��F��B��C��D��E�ֱ��A�γɵĶ�Ԫ�������֪���ٷ�ӦC+G$\stackrel{����}{��}$B+H�ܷų��������ȣ��÷�Ӧ��Ӧ��������ĺ��ӣ� �����Ŀռ乹����ֱ���ͣ�
�����Ŀռ乹����ֱ���ͣ�