题目内容
能说明0.1 mol·L-1的NaHA溶液一定呈酸性的是( )
①稀释时,溶液中c(OH-)增大 ②溶液的pH<7
③溶液中c(Na+)=c(A2-) ④溶液可与等体积等物质的量浓度的NaOH溶液恰好反应
A.①②④ B.①③④ C.①③ D.②④
C
【解析】
试题分析:若NaHA溶液一定呈酸性,则稀释时,溶液中c(H+)减小,根据水的离子积是个常数可知c(OH-)增大,所以①正确;由于水的离子积常数随温度的改变而改变,若温度不是室温,则溶液的pH<7的溶液不一定是酸性溶液,所以②错误;③若溶液中c(Na+)=c(A2-),则电离方程式是NaHA=Na++H++A-,该溶液一定显酸性,所以③正确;④无论该盐是强酸的酸式盐还是弱酸的酸式盐,溶液都可与等体积等物质的量浓度的NaOH溶液恰好反应,与酸式盐的强弱无关,因此不能证明溶液的酸碱性,所以④错误。
考点:考查能够证明NaHA溶液呈酸性的各种说法的知识。

(12分)Ⅰ.已知可逆反应:M(g)+N(g)  P(g)+Q(g) ΔH>0,请回答下列问题:
P(g)+Q(g) ΔH>0,请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为c(M)=1 mol·L-1,c(N)=2.4 mol·L-1。达到平衡后,M的转化率为60%,此时N的转化率为____________。
(2)若反应温度升高,M的转化率__________(填“增大”、“减小”或“不变”)。
(3)若反应温度不变,反应物的起始浓度分别为c(M)=4 mol·L-1,c(N)=a mol·L-1;
达到平衡后,c(P)=2 mol·L-1,a=____________。
Ⅱ.在1.0 L密闭容器中放入0.10molA(g),在一定温度进行如下反应
A(g) B(g)+C(g) △H=+85.1kJ·mol-1
B(g)+C(g) △H=+85.1kJ·mol-1
反应时间(t)与容器内气体总压强(p)的数据见下表:
时间t/h | 0 | 1 | 2 | 4 | 8 | 16 | 20 | 25 | 30 |
总压强p/100kPa | 4.91 | 5.58 | 6.32 | 7.31 | 8.54 | 9.50 | 9.52 | 9.53 | 9.53 |
回答下列问题:
(1)欲提高A的平衡转化率,应采取的措施为 。
(2)由总压强P和起始压强P0计算反应物A的转化率α(A)的表达式为 。
平衡时A的转化率为_ ,列式并计算反应的平衡常数K 。
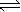 C(g)+D(g)达到平衡,反应过程中正反应速率随时间变化的示意图如图所示.下列说法正确的是( )
C(g)+D(g)达到平衡,反应过程中正反应速率随时间变化的示意图如图所示.下列说法正确的是( )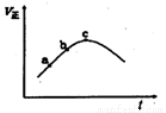
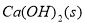
 ,下列说法正确的是( )
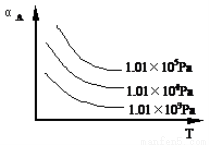
,下列说法正确的是( ) mC(g), A的转化率(αA)与温度(T)、压强的关系如下图所示:
mC(g), A的转化率(αA)与温度(T)、压强的关系如下图所示: