题目内容
7.下列指定反应的离子方程式正确的是( )| A. | 向Ag(NH3)2NO3溶液中加入盐酸:Ag(NH3)2++2H+=Ag++2NH4+ | |
| B. | 向Na2O2中加入足量的水:2Na2O2+2H2O=4Na++4OH-+O2↑ | |
| C. | 向硫酸铝溶液中加入过量氨水:Al3++3OH-=Al(OH)3↓ | |
| D. | 向Ca(HCO3)2溶液中加入澄清石灰水:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
分析 A.反应生成氯化银、硝酸铵;
B.反应生成氢氧化钠和氧气;
C.反应生成氢氧化铝和硫酸铵;
D.反应生成碳酸钙和水.
解答 解:A.向Ag(NH3)2NO3溶液中加入盐酸:Ag(NH3)2++Cl-+2H+=AgCl↓+2NH4+,故A错误;
B.向Na2O2中加入足量的水的离子反应为2Na2O2+2H2O=4Na++4OH-+O2↑,故B正确;
C.向硫酸铝溶液中加入过量氨水的离子反应为Al3++3NH3.H2O=Al(OH)3↓+3NH4+,故C错误;
D.向Ca(HCO3)2溶液中加入澄清石灰水的离子反应为Ca2++HCO3-+OH-=CaCO3↓+H2O,故D错误;
故选B.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质,题目难度不大.

练习册系列答案
相关题目
17.铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与11.2L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸.则消耗铜的质量为( )
| A. | 16 g | B. | 24 g | C. | 32 g | D. | 64g |
18.下列反应都是中学阶段常见的反应,从分类的角度选出不同类型的( )
| A. | 皂化反应 | B. | 焰色反应 | C. | 水解反应 | D. | 钝化反应 |
15.化学与生产生活紧密相关,下列说法正确的是( )
| A. | Na2O2是碱性氧化物,可用于杀菌消毒和供氧剂 | |
| B. | 高纯度单质硅有良好的半导体性能,可用于制备光电池 | |
| C. | 氨气是一种碱性气体,可用碱石灰或CaCl2干燥 | |
| D. | SO2和Cl2都能使品红溶液褪色,两者等体积混合可以增强漂白能力 |
12.能够说明一个可逆反应H2(g)+I2(g)?2HI(g)已达到平衡状态的是( )
| A. | 1 mol H-H键断裂的同时有1 mol H-I键形成 | |
| B. | 1 mol H-H键断裂的同时有2 mol H-I键形成 | |
| C. | 1 mol I-I键断裂的同时有2 mol H--I键形成 | |
| D. | 1 mol H-H键断裂的同时有1 mol I-I键形成 |
19.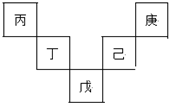 已知丙~庚元素在周期表(前四周期)中的相对位置如下图,其中己的最高氧化物对应水化物有强脱水性,丁原子最外层电子数是最内层电子数的2倍.下列判断错误的是( )
已知丙~庚元素在周期表(前四周期)中的相对位置如下图,其中己的最高氧化物对应水化物有强脱水性,丁原子最外层电子数是最内层电子数的2倍.下列判断错误的是( )
 已知丙~庚元素在周期表(前四周期)中的相对位置如下图,其中己的最高氧化物对应水化物有强脱水性,丁原子最外层电子数是最内层电子数的2倍.下列判断错误的是( )
已知丙~庚元素在周期表(前四周期)中的相对位置如下图,其中己的最高氧化物对应水化物有强脱水性,丁原子最外层电子数是最内层电子数的2倍.下列判断错误的是( )| A. | 丙与戊的原子序数相差28 | |
| B. | 常温下,庚的单质能与水反应产生气体 | |
| C. | 气态氢化物的稳定性:庚<己<戊 | |
| D. | 丁的最高价氧化物可用于制造光导纤维 |
17.如图所示,a、b都是惰性电极,通电一段时间后,a极附近溶液显红色.下列说法中正确的是( )
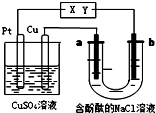

| A. | CuSO4溶液的n(SO42-)保持不变 | B. | U型管中溶液pH值逐渐变小 | ||
| C. | CuSO4溶液的c(Cu2+)逐渐减小 | D. | X是正极,Y是负极 |
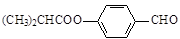 .合成M的一种途径如下:
.合成M的一种途径如下: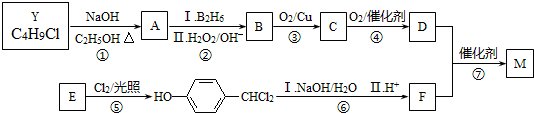
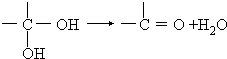
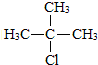 ,D的官能团名为羧基.
,D的官能团名为羧基.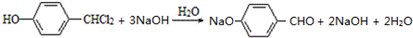 .
.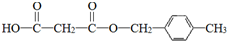 .
.