题目内容
4.25℃时,向水中加入少量碳酸钠固体,得到pH为11的溶液,其主要水解反应的离子方程式为CO32-+H2O=HCO3-+OH-、HCO3-+H2O?H2CO3+OH-,由水电离出的c(OH-)=10-3mol•L-1.分析 碳酸钠为盐,完全电离,碳酸根离子水解分步进行,以第一步为主,不能一步完成,碳酸根离子水解生成碳酸氢根离子和氢氧根离子;pH=11的碳酸钠溶液中氢氧根离子是由水电离产生的,水电离产生的c(H+)等于溶液中水电离出c(OH -),水电离出c(OH -)=10-3mol/L;
解答 解:碳酸钠溶液中CO32-部分水解,分步进行,CO32-+H2O?HCO3-+OH-,以第一步为主,第二步水解为HCO3-+H2O?H2CO3+OH-,pH=11的碳酸钠溶液中氢氧根离子c(OH -)=$\frac{1{0}^{-14}}{1{0}^{-11}}$=10-3mol/L,是由水电离产生的,水电离产生的c(H+)等于溶液中水电离出c(OH -),故水电离出c(OH -)=c(H+)=10-3mol/L,
故答案为:CO32-+H2O=HCO3-+OH-、HCO3-+H2O?H2CO3+OH-;10-3.
点评 本题考查盐类水解的应用\PH计算、溶液酸碱性和离子积常数的计算判断,盐类水解的原理是解题关键,题目难度不大.

为了探究原电池的电极名称不仅与电极材料有关还与电解质溶液有关,某学生做了如下的实验
编号 | 电极材料 | 电解质溶液 | 电子流向 |
① | Mg—Al | HNO3(浓) | Mg→Al |
② | Mg—Al | HCl(aq) | Mg→Al |
③ | Mg—Al | NaOH(aq) | Al→Mg |
④ | Al—Cu | HNO3(浓) | Cu→Al |
根据以上表格内容回答:
(1)实验①中Mg作________(填“正极”或“负极”),发生__________(填“氧化反应”或“还原反应”)。
实验③中Mg作________(填“正极”或“负极”),总反应的离子方程式为: ___。
(2)实验②中Al电极上的电极反应式为______________________。
(3)实验④中正极的电极反应式为_________ _____。
| A. | 在化学反应过程中,发生物质变化的同时不一定发生能量变化 | |
| B. | 需要加热才能发生的化学反应,它可能是吸热反应也可能是放热反应 | |
| C. | 反应产物的总焓大于反应物的总焓时,反应吸热,△H<0 | |
| D. | △H的大小与热化学方程式的计量系数无关 |
| A. | H+、Na+、HCO3-、SO42- | B. | H+、Fe2+、CO32-、Cl- | ||
| C. | Mg2+、K+、SO42?、NO3- | D. | NH4+、Ag+、OH-、Br- |
| A. | PH=12的溶液:Cl-、OH-、K+、Ba2+ | |
| B. | 能使酚酞变红的溶液中:SO42-、NH4+、K+、NO3- | |
| C. | 0.1mol/L的Na2CO3溶液中:K+、Ba2+、NO3-、Cl- | |
| D. | 无色透明溶液中:K+、Na+、MnO4-、Cl- |
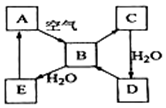 如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.
如图表示某固态单质A及其化合物之间的转化关系(某些产物和反应条件已略去).化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,化合物D是重要的工业原料.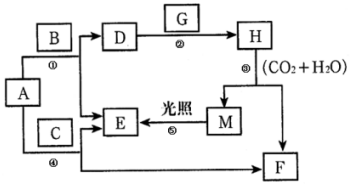 现有A、B、C、D、E、F、G、H、M九种物质,其中A为淡黄色粉末,G为黄绿色气体单质,E为无色气体单质,F的水溶液与石灰水混合可得D的溶液,它们之间的相互转化关系如图,其他与题无关的生成物均已略去.请回答下列问题:
现有A、B、C、D、E、F、G、H、M九种物质,其中A为淡黄色粉末,G为黄绿色气体单质,E为无色气体单质,F的水溶液与石灰水混合可得D的溶液,它们之间的相互转化关系如图,其他与题无关的生成物均已略去.请回答下列问题: